
| A.锌片是正极,铜片上有气泡产生 | B.电流方向是从锌片流向铜片 |
| C.溶液中硫酸的物质的量浓度减小 | D.电解质溶液的pH保持不变 |
科目:高中化学 来源:不详 题型:单选题
| A.负极反应为:14H2O+7O2+28e—=28OH— |
| B.放电一段时间后,负极周围的pH升高 |
| C.理论上消耗1mol C2H6,电路上转移的电子为14mol |
| D.放电过程中,K+向负极移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.X极发生还原反应 |
| B.每生成0.6克CH3COOH,电子转移为0.04 mol |
| C.Y极反应方程式为:O2+4e-+2H2O=4OH— |
| D.质子移向X极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
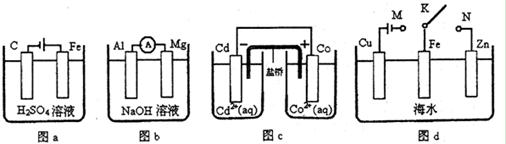
| A.图a中,随着电解的进行溶液中H+的浓度越来越大 |
| B.图b中,Mg电极作电池的负极 |
| C.图c中,发生的反应为Co+Cd2+= Cd+Co2+ |
| D.图d中:K分别与M、N连接,Fe电极均受到保护不会腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X>Y>Z | B.Z>Y>X | C.X>Z>Y | D.Y>X>Z |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
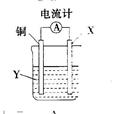
| A.X可以是银或石墨 |
| B.Y是硫酸铜溶液 |
| C.电子从铜电极经外电路流向X电极 |
| D.X极上的电极反应式为:Ag++e-=Ag |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.①③ | C.①④ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
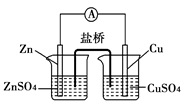
| A.电子从锌电极通过电流计流向铜电极 |
| B.盐桥中的阳离子向硫酸铜溶液中迁移 |
| C.锌电极发生氧化反应,铜电极发生还原反应 |
| D.铜电极上发生的电极反应为2H++2e-===H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com