
【题目】査尔酮类化合物G是黄酮类药物的主要合成中间体,其中一种合成路线如下:
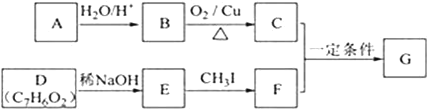
已知以下信息:
①芳香烃A的相对分子质量在100~110之间,1mol A充分燃烧可生成72g水。
②C不能发生银镜反应。
③D能发生银镜反应、可溶于饱和Na2CO3溶液。核磁共振氢谱显示有4种氢。
④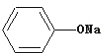 +RCH2I
+RCH2I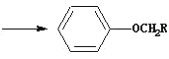
⑤RCOCH3+RˊCHO![]() RCOCH=CHRˊ
RCOCH=CHRˊ
回答下列问题:
(1)A的化学名称为_______。
(2)由B生成C的化学方程式为________。
(3)E的分子式为_______,由E生成F的反应类型为_________。
(4)G的结构简式为______。
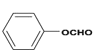
(5)D的芳香同分异构体H既能发生银镜反应,又能发生水解反应,H在酸催化下发生水解反应的化学方程式为________。
【答案】苯乙烯 2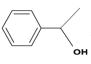 +O2
+O2![]() 2
2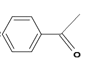 +2H2O C7H5O2Na 取代反应
+2H2O C7H5O2Na 取代反应 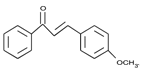
 +H2O
+H2O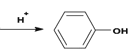 +HCOOH
+HCOOH
【解析】
芳香烃A的相对分子质量在100~110之间,1molA充分燃烧可生成72g水,72g水的物质的量=![]() =4mol,所以1个A分子中含有8个氢原子,A能和水发生加成反应,则A中含有碳碳双键,B中含有羟基,B被氧化后生成C,C不能发生银镜反应,则C中不含醛基,则C中含有羰基,结合A的相对分子质量知,A是苯乙烯,B的结构简式为:
=4mol,所以1个A分子中含有8个氢原子,A能和水发生加成反应,则A中含有碳碳双键,B中含有羟基,B被氧化后生成C,C不能发生银镜反应,则C中不含醛基,则C中含有羰基,结合A的相对分子质量知,A是苯乙烯,B的结构简式为:![]() ,C的结构简式为:
,C的结构简式为:![]() ;D能发生银镜反应说明D中含有醛基,可溶于饱和Na2CO3溶液说明D中含有羧基或酚羟基,核磁共振氢谱显示有4种氢,说明D含有四种类型的氢原子,结合D的分子式知,D是对羟基苯甲醛,D和氢氧化钠溶液反应生成E,E的结构简式为:
;D能发生银镜反应说明D中含有醛基,可溶于饱和Na2CO3溶液说明D中含有羧基或酚羟基,核磁共振氢谱显示有4种氢,说明D含有四种类型的氢原子,结合D的分子式知,D是对羟基苯甲醛,D和氢氧化钠溶液反应生成E,E的结构简式为:![]() ,
,![]() 和碘烷反应生成F,F的结构简式为:
和碘烷反应生成F,F的结构简式为:![]() ,C和F反应生成G,结合题给信息知,G的结构简式为:
,C和F反应生成G,结合题给信息知,G的结构简式为: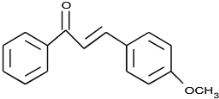 。
。
(1)通过以上分析知,A是苯乙烯;
(2)在加热、铜作催化剂条件下,B被氧气氧化生成C,反应方程式为: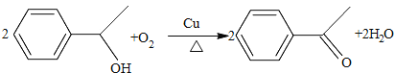 ;
;
(3)通过以上分析知,E的分子式为:C7H5O2Na,E发生取代反应生成F;
(4)通过以上分析知,G的结构简式为: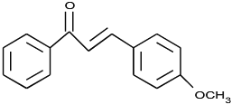 ;
;
(5)D的芳香同分异构体H既能发生银镜反应,又能发生水解反应,说明H中含有苯环、醛基和酯基,所以H是甲酸苯酯,H在酸催化下发生水解反应的化学方程式为: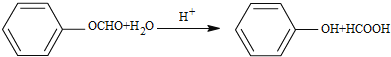 。
。


科目:高中化学 来源: 题型:
【题目】下列有关化合物X的叙述正确的是

A. X分子只存在2个手性碳原子
B. X分子能发生氧化、取代、消去反应
C. X分子中所有碳原子可能在同一平面上
D. 1 mol X与足量NaOH溶液反应,最多消耗3 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个固定容积的密闭容器中通入amolN2与bmolH2的混合气体,保持温度不变,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g)。
2NH3(g)。
(1)若反应到某时刻t时,n(N2)=9mol,n(NH3)=2mol,则a=____mol;
(2)反应达平衡时,混合气体的体积为448L(标况下),其中NH3的含量(体积分数)为25%,平衡时NH3的物质的量____;
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比、下同),n(始)∶n(平)=____;
(4)原混合气体中,a∶b=_____;
(5)平衡混合气体中,n(N2)∶n(H2)∶n(NH3)=_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对一种未知有机物的结构测定,往往需要多种复杂方法相结合,一般来说,主要包括以下几个方面:①相对分子质量;②元素组成(种类和比例);③该有机物的各种性质的研究;④结构的确定。
(1)相对分子质量的确定一般有质谱法,蒸气密度法等。蒸气密度法是指一定条件下将有机物气化,测定该条件下的密度,利用气态方程式计算相对分子质量。蒸气密度法的要求是该有机物在______。如果沸点过高,可以采用________方法。质谱法是在一定条件下让有机物失去电子变成阳离子,测其相对分子质量。该过程中,复杂的有机物分子往往变成小的片断,如C4H10断裂成CH3CH2CH2+、CH3CH2+、CH3+、CH3CH2CH2CH2+等,其式量最大的就是其相对分子质量。该法测定某有机物A质谱中显示相对分子质量最大是72。
(2)组成元素的测定往往采用元素分析仪,以前也常用燃烧法。称取3.6 gA,跟足量氧气充分燃烧后通过浓硫酸,浓硫酸增重5.4 g,剩余气体通过碱石灰,碱石灰增重11 g,则该有机物的分子式为________。
(3)核磁共振谱常用氢谱和碳谱,它主要测定分子中具有不同特点的C或H的种类与比例。如对于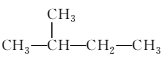 ,经测定,C谱有四个峰,其数值高低比例为2∶1∶1∶1;H谱有四个峰,其数值高低比例为1∶2∶3∶6。有机物A碳谱有两个峰,峰高比为4∶1。氢谱有一个峰。试写出有机物A的结构简式________。
,经测定,C谱有四个峰,其数值高低比例为2∶1∶1∶1;H谱有四个峰,其数值高低比例为1∶2∶3∶6。有机物A碳谱有两个峰,峰高比为4∶1。氢谱有一个峰。试写出有机物A的结构简式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M的结构简式如图,有关M的下列叙述中正确的是

A. 可与H2反应,1 molM最多消耗1 molH2
B. 可与浓溴水反应,1molM最多消耗4 molBr2
C. 可与NaOH溶液反应,1 mol M最多消耗3 molNaOH
D. 常温下,M在水中的溶解度小于苯酚在水中的溶解度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同条件下进行化学反应2A(g)=B(g)+D(g),B、D起始浓度均为0,反应物A的浓度(mol/L)随反应时间的变化情况如下表:
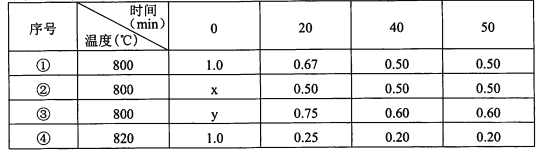
下列说法不正确的是
A.①中B在0~20 min平均反应速率为8.25xl0-3moI.L-l.min-l
B.②中K=0.25,可能使用了催化剂
C.③中y= 1.4 moI.L-l
D.比较①、④可知,该反应为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:X(g)+2Y(g) ![]() 3Z(g)△H=-akJmol﹣1(a>0)。下列说法不正确的是
3Z(g)△H=-akJmol﹣1(a>0)。下列说法不正确的是
A.升高反应温度,逆反应速率增大,正反应速率减小
B.达到化学平衡状态时,X、Y、Z的浓度不再发生变化
C.1molX和2molY完全反应生成3mol的Z,放出akJ的热量
D.0.1molX和0.2molY充分反应生成Z的物质的量一定小于0.3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家首次抓住“兔耳朵”解密催化反应“黑匣子”。图a是TiO2结构图,图b是TiO2吸附H2O后形成“兔耳朵”的结构图,图c是图b的俯视图。下列叙述错误的是
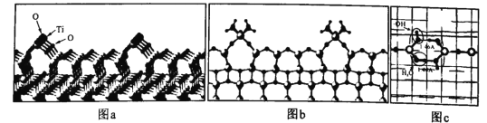
A.由图a可知,每隔4个Ti原子会有一列凸起
B.由图b可知,凸起位置上的Ti原子是反应的活性位点
C.由图c可知,水分子和羟基之间靠共价键结合
D.将CO引入体系,通过观察凸起结构变化,证实水煤气变换催化反应的发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程。已知反应:N2(g)+3H2(g)2NH3(g)△H。有关键能数据如下:
化学键 | H-H | N-H | N≡N |
键能)kJ/mol) | 436 | 391 | 945 |
根据表中所列键能数据可得△H=____________。
(2)已知:CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H= +49.0kJ/mol
CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g)△H= -192.9kJ/mol
O2(g)=CO2(g)+2H2O(g)△H= -192.9kJ/mol
已知水的气化热为44.0kJ/mol,表示氢气燃烧热的热化学方程式为______________。
(3)已知化学反应A(g)+B(g)C(g)+D(g),900℃时向一个体积为2L的密闭容器中充入0.20mol A和0.80mol B,2s时达到平衡,A的浓度变化0.05mol/L,则A的平均反应速率v(A) =________,平衡时B的转化率为____ ,C的体积百分数为_______ 。
(4)CO、H2可用于合成甲醇和甲醚,其反应为(m、n均大于![]() ):
):
反应①:CO(g)+2H2(g)CH3OH(g)△H=-m kJ/mol
反应②:2CO(g)+4H2(g)CH3OCH3(g)+H2O(g)△H=-n kJ/mol
反应③:2CH3OH(g)CH3OCH3(g)+H2O(g)△H<0
根据上述的热化学方程式可以判断则2m_____n(填“大于”、“小于”、“等于”或“无法确定”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com