
硫的化合物在生产和科研中发挥着重要作用。
(1)SO2Cl2常用于制造医药品、染料、表面活性剂等。已知:SO2Cl2(g) SO2(g)+Cl2(g) △H=+97.3 kJ·mol-1。某温度时向体积为1 L的恒容密闭容器中充入0. 20mol SO2Cl2,达到平衡时,容器中含0.18mol SO2,则此过程反应吸收的热量为_____ kJ,该温度时反应的平衡常数为_____。将上述所得混合气体溶于足量BaCl2溶液中,最终生成沉淀的质量为_______。
SO2(g)+Cl2(g) △H=+97.3 kJ·mol-1。某温度时向体积为1 L的恒容密闭容器中充入0. 20mol SO2Cl2,达到平衡时,容器中含0.18mol SO2,则此过程反应吸收的热量为_____ kJ,该温度时反应的平衡常数为_____。将上述所得混合气体溶于足量BaCl2溶液中,最终生成沉淀的质量为_______。
(2)工业上制备硫酸的过程中存在反应:2SO2(g)+O2(g) 2SO3(g) △H=-198kJ·mol-1,400℃,1.01×105Pa,向容积为2L的恒容密闭容器中充入一定量 SO2和O2,n(SO3)和n(O2)随时间的变化曲线如图所示。
2SO3(g) △H=-198kJ·mol-1,400℃,1.01×105Pa,向容积为2L的恒容密闭容器中充入一定量 SO2和O2,n(SO3)和n(O2)随时间的变化曲线如图所示。
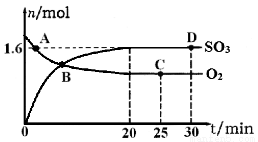
①0~20min反应的平均速率υ(O2)=___________。
②下列叙述正确的是 。
a.A点υ正(SO2)>υ逆(SO2)
b.B点处于平衡状态
c.C点和D点n(SO2)相同
d.其它条件不变,500℃时反应达平衡,n(SO3)比图中D点的值大
(3)工业上用Na2SO3溶液吸收烟气中的SO2。将烟气通入1.0 mol·L-1的Na2SO3溶液,当溶液pH约为6时,Na2SO3溶液吸收SO2的能力显著下降,应更换吸收剂。此时溶液中c (SO32-)的浓度是0.2 mol·L-1,则溶液中c(HSO3-)是__mol·L-1。
(1)17.5 1.62 46.6g
(2)0.02mol/(L·min) ac
(3)1.6mol/L
【解析】(1)达到平衡时,容器中含0.18mol SO2,则根据热化学方程式可知,此过程反应吸收的热量为97.3 kJ·mol-1×0.18mol=17.5kJ。根据方程式可知
SO2Cl2(g) SO2(g)+Cl2(g)
SO2(g)+Cl2(g)
起始浓度(mol/L) 0.20 0 0
转化浓度(mol/L) 0.18 0.18 0.18
平衡浓度(mol/L) 0.02 0.18 0.18
所以该温度下反应的平衡常数K= =1.62。
=1.62。
所得混合气体溶于足量BaCl2溶液中,发生反应SO2+Cl2+2H2O=H2SO4+2HCl,所以促使平衡持续向正反应方向进行,因此最终生成沉淀的物质的量是0.20mol,则硫酸钡的质量为0.20mol×232g/mol=46.6g。
(2)①根据图像可知20min时三氧化硫的物质的量是1.6mol,则消耗氧气的物质的量是0.8mol,浓度是0.4mol/L,所以0~20min反应的平均速率υ(O2)=0.4mol/L÷20min=0.02mol(L·min);
②a.根据图像可知A点反应没有达到平衡状态,平衡向正反应方向进行,则υ正(SO2)>υ逆(SO2),a正确;b.B点物质的浓度仍然是变化的,反应没有处于平衡状态,b不正确;c.C点和D点均是相同条件下的平衡状态,因此n(SO2)相同,c正确;d.正方应是放热反应,其它条件不变,升高温度平衡向逆反应方向移动,所以500℃时反应达平衡,n(SO3)比图中D点的值小,d不正确,答案选ac。
(3)溶液中c (SO32-)的浓度是0.2 mol·L-1,则消耗c (SO32-)的浓度=1.0mol/L-0.2mol/L=0.8mol/L,因此根据方程式SO32-+SO2+H2O=2HSO3-可知溶液c(HSO3-)=0.8mol/L×2=1.6mol/L


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源:2014高考名师推荐化学NA与粒子(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值。下列说法正确的是
A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA
B.常温常压下,18g H2O含有的原子总数为3NA
C.标准状况下,11.2LCH3CH2OH中含有分子的数目为0.5NA
D.常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测8 题型:选择题
分子式为C5H12O的醇与和它相对分子质量相同的一元羧酸进行酯化反应,生成的酯共有(不考虑立体异构)几种
A.15 B.16 C.17 D.18
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测7 题型:选择题
下列说法正确的是
A.短周期元素形成离子后,最外层均达8电子稳定结构
B.多电子原子中,在离核较近的区域运动的电子能量较低
C.非金属元素组成的化合物中只有共价键
D.HF、HCl、HBr、HI的热稳定性和还原性依次增强
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测7 题型:选择题
工业上常将铬镀在其他金属表面,同铁、镍组成各种性质的不锈钢,在下图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电极上无气体产生,铬电极上产生大量有色气体,则下列叙述正确的是

A.图1为原电池装置,Cu电极上产生的是O2
B.图2装置中Cu电极上发生的电极反应式为:Cu-2e-===Cu2+
C.由实验现象可知:金属活动性Cu>Cr
D.两个装置中,电子均由Cr电极流向Cu电极
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测6 题型:选择题
下列有关化学用语表示正确的是
A 二氧化硅的分子式:SiO2
B质子数为53,中子数为78的碘原子:
C甲基的电子式:
D邻羟基苯甲酸的结构简式:
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测6 题型:选择题
下列说法中不正确的是
A.光导纤维、硝化纤维、铜氨纤维、玻璃纤维的主成分都是糖类
B.生理盐水、葡萄糖注射液都不能产生丁达尔效应现象,不属于胶体
C.红外光谱仪可用于测定化合物的官能团、1H核磁共振仪可确定H所处的化学环境
D.用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可到达水果保鲜的目的
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测5 题型:选择题
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍。下列说法正确的是

A.元素Y和元素Z的最高正化合价相同
B.单核阴离子半径的大小顺序为:r(W)>r(Y)>r(Z)
C.气态氢化物稳定性:X <Y<Z<W
D.元素W的最高价氧化物对应的水化物是强酸
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测3 题型:选择题
下列各组离子一定能大量共存的是
A.加入铝粉有氢气产生的溶液中Na+ 、K+ 、SO42-、Cl- 、HCO3-
B.含有大量硝酸根离子的溶液中H+ 、Fe2+ 、SO42-、Cl-
、SO42-、Cl-
C.常温下,c(H+)/c(OH-) = 1×10-10 的溶液中NH4+ 、K+ 、Ca2+ 、Cl-
D. 常温下pH=1的溶液中:MnO4-、NO3-、SO42-、Na+、Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com