
【题目】在xR2++yH++O2=mR3++nH2O的离子方程式中,对m和R3+判断正确的是( )
A.m=4,R3+是氧化产物
B.m=2y,R3+是氧化产物
C.m=2,R3+是还原产物
D.m=y,R3+是还原产物
科目:高中化学 来源: 题型:
【题目】1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125 ℃,反应装置如图。下列对该实验的描述错误的是( )

A. 不能用水浴加热
B. 长玻璃管起冷凝回流作用
C. 提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
D. 加入过量乙酸可以提高1—丁醇的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯仿(CHCl3 , 非电解质)在空气中能发生缓慢氧化,生成剧毒物质光气(COCl2 , 非电解质),化学方程式为2CHCl3+O2=2COCl2+2HCl.检验氯仿是否被氧化应选用的试剂是( )
A.水
B.NaOH溶液
C.酚酞溶液
D.硝酸酸化的硝酸银溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具,下列化学用语中,正确的是
A. NH4+的水解反应离子方程式:NH4++H2O![]() NH3H2O+H+
NH3H2O+H+
B. 在AgCl悬浊液中加入KI溶液充分振荡:Ag++I-=AgI↓
C. 镀铜时,阳极的电极反应式为:Cu2++2e-═Cu
D. 某反应△H<0,则该反应在任意条件下均可自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 对平衡体系H2(g)+I2(g)![]() 2HI(g)加压后,混合气体的颜色加深
2HI(g)加压后,混合气体的颜色加深
B. 用稀盐酸洗涤AgCl沉淀比用等体积的蒸馏水洗涤损失的AgCl少
C. 实验室可用排饱和食盐水的方法收集氯气
D. 工业合成三氧化硫的过程中使用过量的氧气,以提高二氧化硫的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.经测定乙醇的化学式是C2H6O,由于有机物普遍存在同分异构现象,推测乙醇的结构可能是下列两种之一。

为测定其结构,应利用物质的特殊性进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,请甲、乙、丙、丁4位同学利用如下图的装置进行实验,确定乙醇的结构。

(1)同学甲得到一组实验数据如表:
乙醇的物质的量/mol | 氢气的体积/L |
0.10 | 1.12(标准状况) |
根据以上数据推断乙醇的结构为______(用Ⅰ、Ⅱ表示),理由为____________;
(2)同学乙分别准确称量4.60 g乙醇进行多次实验,结果发现以排在量筒内水的体积作为生成的H2体积,换算成标准状况后都小于1.12 L。如果忽略量筒本身及乙同学读数造成的误差,乙同学认为可能是由于样品中含有少量水造成的,你认为正确吗?______(填“正确”或“不正确”)。请说明理由__________________________________________________________________。
(3)同学丙认为实验成功的关键有:①装置气密性要良好;②实验开始前准确确定乙醇的量;③钠足量;④广口瓶内水必须充满;⑤氢气体积的测算方法正确、数据准确。其中,正确的有_________________(填序号)。
(4)同学丁不想通过称量乙醇的质量来确定乙醇的量,那么还需要知道的数据是________。
(5)实验后,4名同学从乙醇的可能结构分析入手,对乙醇和钠的量的关系进行了讨论,如果乙醇的物质的量为n mol,那么对钠的物质的量的取值要求,必须是____________。
II.已知A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。

请回答下列问题:
(1)A的结构简式为______________________,在农业上可以用于________________。
(2)E的结构简式为___________________;B、D分子与金属钠反应的化学方程式为____________________________、____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾天气严重影响人们的生活质量,其中氮氧化物和硫氧化物是造成雾霾天气的主要原因之一。消除氮氧化物和硫氧化物有多种方法。
(1)氮、氧元素非金属性较强的是________。
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:

①由图1可知SCR技术中的氧化剂为________。
②用Fe作催化剂时,在氨气足量的情况下,不同c(NO2)/c(NO)对应的脱氮率如图2所示,脱氮效果最佳的c(NO2)/c(NO)=________。
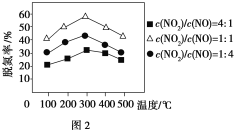
(3)海水具有良好的吸收SO2的能力,其吸收过程如下:
①SO2溶于海水生成H2SO3,H2SO3最终会电离出SO![]() ,SO
,SO![]() 可以被海水中的溶解氧氧化为SO
可以被海水中的溶解氧氧化为SO![]() 。海水的pH会________(填“升高”“不变”或“降低”)。
。海水的pH会________(填“升高”“不变”或“降低”)。
②SO2和O2在H2SO4溶液中可以构成原电池,其负极反应式是_____________________。
(4)碲(Te)为第ⅥA族元素,是当今高新技术新材料的主要成分之一。工业上可将SO2通入TeCl4的酸性溶液中进行“还原”得到碲,该反应的化学方程式是___________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com