
| A. | H2O2的电子: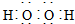 | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | S2-离子的结构示意图: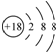 | |
| D. | FeSO4的电离方程式:FeSO4═Fe3++SO42- |
分析 A.H2O2中两个氢原子分别与两个氧原子通过共用一对电子结合,两个氧原子之间通过共用1对电子结合;
B.乙烯分子中两个碳原子之间通过共用2对电子形成一个碳碳双键;
C.硫离子的核电荷数为16,核外电子总数为18,最外层含有8个电子,核电荷数18表示错误;
D.FeSO4电离为Fe2+和SO42-.
解答 解:A.H2O2为共价化合物,分子中存在两个氧氢键和一个O-O键,H2O2的电子式为 ,故A正确;
,故A正确;
B.乙烯含有碳碳双键,结构简式为CH2=CH2,故B错误;
C.硫离子核外存在18个电子,核内有16个质子,最外层达到8电子稳定结构,其离子结构示意图为: ,故C错误;
,故C错误;
D.FeSO4属于强电解质,完全电离为Fe2+和SO42-,电离方程式为:FeSO4=Fe2++SO42-,故D错误;
故选A.
点评 本题考查了化学用语书写,掌握相关化学用语的书写规范即可解答,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 水解反应 | 平衡常数(K) |
| Fe3++3H2O?Fe(OH)3+3H+ | 7.9×10-4 |
| Fe2++2H2O?Fe(OH)2+2H+ | 3.2×10-10 |
| Cu2++2H2O?Cu(OH)2+2H+ | 3.2×10-7 |
| 实验内容 | 实验现象 |
| 甲同学的实验方案 | 溶液逐渐变成蓝绿色,pH略有上升 |
| 乙同学的实验方案 | 无明显现象,pH没有明显变化. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
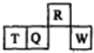 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A. | 最简单气态氢化物的热稳定性:R>Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W | |
| C. | 原子半径:T>Q>R | |
| D. | 含T的盐溶液一定能与碱反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 504mL | B. | 112mL | C. | 336mL | D. | 224mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20Ne和22Ne互为同位素 | |
| B. | 液氯和氯水是同一种物质 | |
| C. | 金刚石、石墨和富勒烯互为同分异构体 | |
| D. | 碘单质和碘蒸气互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 冰晶石能降低Al2O3的熔点,用Al2O3炼铝时加入它可减少能耗 | |
| B. | Mg在空气中燃烧时发出耀眼的白光,可用于制造信号弹 | |
| C. | 氧化钠能与H2O、CO2反应,可用作漂白剂和供氧剂 | |
| D. | 常温时浓硝酸与铁不反应,可用铁桶贮存浓硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

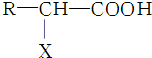 ,X的名称为氨基.
,X的名称为氨基. )易水解,其水解反应的产物为乙酸和
)易水解,其水解反应的产物为乙酸和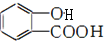 (填结构简式).
(填结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ≥7 | B. | ≤7 | C. | 一定等于7 | D. | 可能大于7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 检测次数 | 溶液中检测出的物质 |
| 第一次 | MgSO4、NaNO3、KNO3、 |
| 第二次 | Mg (NO3)2、KNO3、Na2SO4 |
| 第三次 | Mg (NO3)2、Ba(NO3)2、Na2SO4 |
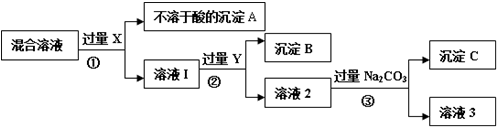
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com