
【题目】用98﹪浓硫酸配制200 mL 0. 5mol/L的硫酸溶液,一定需要使用的玻璃仪器是
①玻璃棒 ②烧杯 ③烧瓶 ④量筒 ⑤容量瓶
A. ①②③ B. ①②④ C. ①②④⑤ D. ③④⑤
科目:高中化学 来源: 题型:
【题目】在容积为2 L的密闭容器中进行如下反应:A(g)+2B(g)![]() 3C(g)+2D(g),开始时A为4 mol,B为6 mol;5 min末时测得C的物质的量为3 mol。请计算:
3C(g)+2D(g),开始时A为4 mol,B为6 mol;5 min末时测得C的物质的量为3 mol。请计算:
(1)5min末A的物质的量浓度___________________;
(2)5min内D的平均化学反应速率____________________;
(3)B的转化率_____________________________;
(4)反应后容器中的总压强与反应前总压强之比为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释实际应用原理的表达式中,不正确的是
A. 用排饱和食盐水法收集Cl2: Cl2+H2O![]() H++Cl-+HClO
H++Cl-+HClO
B. H2燃烧热的热化学方程式:H2 (g)+1/2O2 (g) =H2O(1) △H=-285.8kJ·mol-1
C. 热的氢氟酸酸性增强:HF+H2O= H3O++F- △H>0
D. 用 TiCl4制备 TiO2:TiCl4+(x+2)H2O (过量)![]() TiO2·xH2O↓+4HCl
TiO2·xH2O↓+4HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化学家侯德榜(如图)改进国外的纯碱生产工艺,生产流程可简要表示如图: 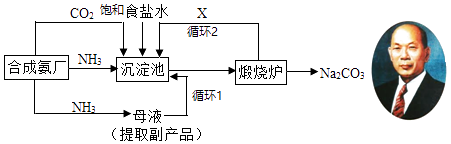
该生产纯碱的方法称联合制碱法或侯德榜制碱法联合制碱法或侯德榜制碱法,在制得纯碱的同时,还可得到一种副产品.
(1)上述沉淀池中发生的化学反应方程式是 , 实验室分离出沉淀的操作是 , 该操作使用的玻璃仪器有;
(2)写出上述流程中X物质的分子式;
(3)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了的循环(填上述流程中的编号1、2);
(4)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,还需要的试剂有;
(5)向母液中通氨气,加入细小食盐颗粒,冷却析出副产品.通氨气的作用有 .
A.增大NH4+的浓度,使NH4Cl更多地析出
B.使NaHCO3更多地析出
C.使NaHCO3转化为Na2CO3 , 提高析出的NH4Cl纯度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.1L0.1mol·L—1的氨水中含有的NH3分子数为0.1NA
B.标准状况下,2.24L的CCl4中含有的C—Cl键数为0.4NA
C.常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4 NA
D.常温常压下,Na2O2与足量CO2反应生成2.24L O2,转移电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于铝的叙述不正确的是
A. 铝是地壳中含量最多的元素
B. 在常温下,铝能与NaOH溶液反应
C. 铝是一种比较活泼的金属
D. 在化学反应中,铝容易失去电子,是还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com