
| A. | 麻黄碱适应于医治因葡萄球菌和链球菌引起的血毒症 | |
| B. | 胃酸过多,出现反胃、吐酸等现象时,可服用小苏打 | |
| C. | 感冒发热头痛时,服用阿司匹林 | |
| D. | 因葡萄球菌等引起的发炎,注射青霉素 |
分析 A.麻黄碱为拟肾上腺素药,能兴奋交感神经,药效较肾上腺素持久,口服有效,它能松弛支气管平滑肌、收缩血管,有显著的中枢兴奋作用;
B.胃酸的主要成分是盐酸,盐酸能和小苏打反应;
C.阿司匹林是解热镇痛药;
D.青霉素是抗生素.
解答 解:A.麻黄碱能松弛支气管平滑肌、收缩血管,有显著的中枢兴奋作用,不适合于医治因葡萄球菌和链球菌等引起的血毒症,故A错误;
B.胃酸的主要成分是盐酸,盐酸能和小苏打反应,所以胃酸过多时,可服用适量的小苏打,故B正确;
C.阿司匹林是解热镇痛药,不能预防感冒,故C正确;
D.青霉素是抗生素,能杀死细菌,故D正确.
故选A.
点评 本题考查药物的主要成分和疗效,难度不大,注意麻黄碱有显著的中枢兴奋作用,是国际奥委会严格禁止使用的兴奋剂.


科目:高中化学 来源: 题型:选择题
| A. | 乙烯和苯分子中均含有碳碳双键,二者都能发生加成反应 | |
| B. | 汽油、煤油、植物油均为含碳、氢、氧三种元素的化合物 | |
| C. | 苯、乙醇和乙酸都能发生取代反应 | |
| D. | 羊毛、蚕丝和棉花等天然高分子材料的主要成分都是蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相对原子质量和电子数 | B. | 电子层数和最外层电子数 | ||
| C. | 电子层数和次外层电子数 | D. | 相对原子质量和最外层电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L的Na2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| B. | pH=11的氨水与pH=3的硫酸各1L混合后,C(NH4+)>2c(SO42-) | |
| C. | pH=11的氨水与pH=11的醋酸钠溶液,由水电离出的c(H+)相等 | |
| D. | pH相同的①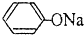 溶液②CH3COONa溶液中的c(Na+):①>② 溶液②CH3COONa溶液中的c(Na+):①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验氯乙烷中的氯元素,水解后再用硫酸酸化 | |
| B. | 为了增强KMnO4溶液的氧化能力,用浓盐酸酸化 | |
| C. | 为了抑制Fe2+的水解,用稀硝酸酸化 | |
| D. | 检验溶液中是否含有SO42-时,先用盐酸酸化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
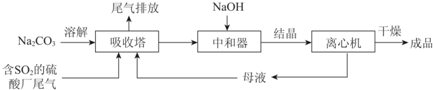
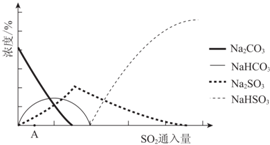
| 资料显示: Ⅰ.Na2SO3在33℃时溶解度最大,将其饱和溶液加热至33℃以上时,由于溶解度降低会析出无水Na2SO3,冷却至33℃以下时析出Na2SO3•7H2O; Ⅱ.无水Na2SO3在空气中不易被氧化,Na2SO3•7H2O在空气中易被氧化. |
 2Na+ (aq)+SO32- (aq),NaOH过量使c(Na+)增大,上述平衡逆向移动.
2Na+ (aq)+SO32- (aq),NaOH过量使c(Na+)增大,上述平衡逆向移动.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
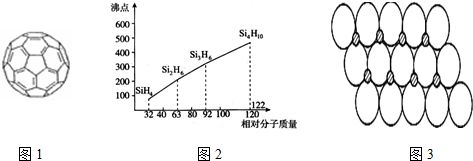
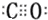 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com