
| A. | NaOH | B. | Al(OH)3 | C. | LiOH | D. | RbOH |
分析 金属的金属性越强,其最高价氧化物的水化物碱性越强,同一周期元素,元素的金属性随着原子序数增大而减弱,同一主族元素,元素的金属性随着原子序数增大而增强,据此分析解答.
解答 解:金属的金属性越强,其最高价氧化物的水化物碱性越强,同一周期元素,元素的金属性随着原子序数增大而减弱,同一主族元素,元素的金属性随着原子序数增大而增强,所以金属性Rb>K>Na>Mg>Al,所以强碱碱性介于KOH和Mg(OH)2之间的是NaOH,故选A.
点评 本题考查金属氧化物的水化物碱性强弱判断,明确金属的金属性强弱与其最高价氧化物的水化物碱性强弱关系即可解答,知道金属性强弱判断方法,题目难度不大.


 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 铝合金表面有致密氧化膜遇强碱不会被腐蚀 | |
| B. | 海轮外壳上装锌块可减缓腐蚀 | |
| C. | 高纯度的SiO2由于可以导电因此可用作光导纤维 | |
| D. | SO2、CO2和NO2都是可形成酸雨的气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
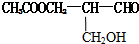 具有光学活性,当它发生下列反应后生成的有机物仍然一定具有光学活性的是( )
具有光学活性,当它发生下列反应后生成的有机物仍然一定具有光学活性的是( )| A. | 与甲酸发生酯化反应 | B. | 与NaOH溶液共热 | ||
| C. | 与氧气发生催化氧化 | D. | 在催化剂存在下与H2作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍型如图所示,下列有关叙述正确的是( )
某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍型如图所示,下列有关叙述正确的是( )| A. | ①②③ | B. | ①③④ | C. | ③④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的电子式  | |
| B. | Cl-的结构示意图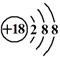 | |
| C. | 8个中子的碳原子的核素符号:${\;}_{6}^{14}$C | |
| D. | HF的电子式: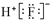 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第ⅠA族元素铯的两种位素${\;}_{\;}^{137}$Cs比${\;}_{\;}^{133}$Cs多4个质子 | |
| B. | 第ⅦA族元素从上到下,其氢化物的还原性逐渐减弱 | |
| C. | 同主族元素原子半径越大,单质的熔点越高 | |
| D. | 同周期元素(除0族元素外)从左到右,简单阴离子半径逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,0.1mol•L-1的NH4NO3溶液中氮原子数为0.2NA | |
| B. | 标准状况下,5.6L CCl4含有的分子数为0.25 NA | |
| C. | 在标准状况下,2.8g N2和2.24LCO所含质子数均为1.4NA | |
| D. | 常温下,1 L pH=1的硫酸溶液中含有的H+数为0.05NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com