
| A. | 液化石油气主要含乙烯、丙烯和甲烷 | |
| B. | 限制氟利昂的使用是为了保护大气臭氧层 | |
| C. | 在船身适当位置装锌块可以避免船体遭受腐蚀 | |
| D. | 工业上冶炼像钠、钙、镁、铝这样的活泼金属,需采用电解法 |
分析 A.液化石油气是碳原子数在3-4的烷烃、环烷烃的混合物;
B.氟利昂可破坏臭氧层;
C.船身适当位置装锌块,构成原电池,Zn为负极;
D.活泼金属利用电解法冶炼.
解答 解:A.液化石油气是通过石油分馏得到,而石油中不含烯烃,故液化石油气是烷烃、环烷烃的混合物,不含乙烯、丙烯,故A错误;
B.氟利昂可破坏臭氧层,臭氧层可保护人类免受紫外线的辐射,则限制氟利昂的使用是为了保护大气臭氧层,故B正确;
C.船身适当位置装锌块,构成原电池,Zn为负极,可以避免船体遭受腐蚀,为牺牲阳极的阴极保护法,故C正确;
D.活泼金属利用电解法冶炼,则工业上冶炼像钠、钙、镁、铝这样的活泼金属,需采用电解法,故D正确;
故选A.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生反应、化学与生活的联系为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 碱性氧化物:Na2O Na2O2 A12O3 | B. | 酸性氧化物:CO SiO2 SO2 | ||
| C. | 盐:NH4NO3 KA1(SO4)2 KHSO4 | D. | 碱:烧碱 纯碱 碱石灰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式:CH2CH2 | B. | 苯的实验式:CH | ||
| C. | CaC2的电子式: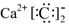 | D. | -CH2CH3的名称是乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CH3COOH溶液至终点,消耗NaOH溶液的体积相等 | |
| B. | 浓度均为0.1 mol•L-1的 HCOONa和NaCl溶液中阴离子的物质的量浓度之和:前者大于后者 | |
| C. | 0.2 mol•L-1 CH3COONa 与 0.1 mol•L-1盐酸等体积混合后的溶液 (pH<7)中,某些粒子浓度大小关系:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| D. | 0.4 mol•L-1 HCOOH 与 0.2 mol•L-1 NaOH 等体积混合后的溶液中,某些粒子浓度大小关系:c(HCOO-)+c(OH-)=c(HCOOH)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的 | |
| B. | 日常生活中,卤水点豆腐、花生中提取花生油、海水晒盐都是物理变化 | |
| C. | 食品保鲜膜、塑料水杯等生活用品的主要成分是聚氯乙烯 | |
| D. | 铝比铁活泼,所以一般情况下,铁制品比铝制品更耐腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图,曲线为可逆反应A(g)+2B(g)?2C(g) 正反应为吸热反应的平衡移动关系曲线,下列说法正确的是( )
如图,曲线为可逆反应A(g)+2B(g)?2C(g) 正反应为吸热反应的平衡移动关系曲线,下列说法正确的是( )| A. | a<b,y轴指B的质量分数 | B. | a>b,y轴指C的质量分数 | ||
| C. | a<b,y轴指A的转化率 | D. | a>b,y轴指A的体积分数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑ | B. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | ||
| C. | 2MgO$\frac{\underline{\;\;△\;\;}}{\;}$2Mg+O2↑ | D. | MgCl2$\frac{\underline{\;电解\;}}{熔融}$Mg+Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
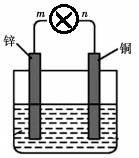 将质量均为100g的锌片和铜片用导线与灯泡串联浸入盛有500mL 2mol•L-1稀硫酸溶液的1.5L容器中构成如图装置.
将质量均为100g的锌片和铜片用导线与灯泡串联浸入盛有500mL 2mol•L-1稀硫酸溶液的1.5L容器中构成如图装置.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com