

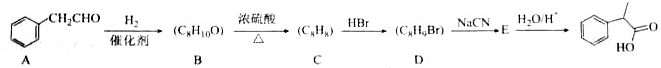
 .
.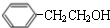 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$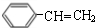 +H2O;C→D的反应类型为加成反应
+H2O;C→D的反应类型为加成反应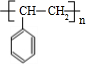 .
. 分析 D中-Br被-CN取代生成E,E发生水解反应得到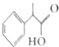 ,则E为
,则E为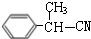 、D为
、D为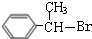 ,逆推可知C为
,逆推可知C为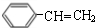 ,B为
,B为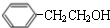 .
.
解答 解:D中-Br被-CN取代生成E,E发生水解反应得到 ,则E为
,则E为 、D为
、D为 ,逆推可知C为
,逆推可知C为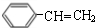 ,B为
,B为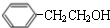 .
.
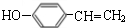
(1)遇FeCl3溶液显紫色且苯环上有两个取代基的A的同分异构体,含有酚羟基、-CH=CH2,有邻、间、对3种,其中苯环上核磁共振氢谱为2组峰且面积比为1:1的同分异构体的结构简式为 ,
,
故答案为:3; ;
;
(2)B→C的化学方程式为: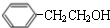 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$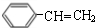 +H2O,C→D是苯乙烯与HBr发生加成反应,
+H2O,C→D是苯乙烯与HBr发生加成反应,
故答案为: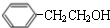 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$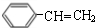 +H2O;加成反应;
+H2O;加成反应;
(3)有机物C为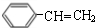 ,名称为苯乙烯,C在一定条件下可以生成高聚物F,F的结构简式为
,名称为苯乙烯,C在一定条件下可以生成高聚物F,F的结构简式为  ,
,
故答案为:苯乙烯; .
.
点评 本题考查有机物推断、有机物的结构与性质、同分异构体书写、有机反应类型等,根据反应条件进行推断,熟练掌握官能团的性质与转化,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 172.5 kJ | B. | 1 149 kJ | C. | 283 kJ | D. | 517.5 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
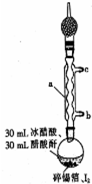 四碘化锡是一种橙红色结晶,熔点为144.5℃,沸点为364℃,不溶于冷水,溶于醇、苯、氯仿等,遇水易水解,常用作分析试剂和有机合成试剂.实验室制备四碘化锡的主要步骤如下:
四碘化锡是一种橙红色结晶,熔点为144.5℃,沸点为364℃,不溶于冷水,溶于醇、苯、氯仿等,遇水易水解,常用作分析试剂和有机合成试剂.实验室制备四碘化锡的主要步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
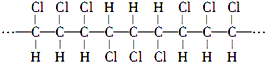 ;下列说法正确的是(双选)( )
;下列说法正确的是(双选)( )| A. | 聚合物的分子式是C3H3Cl3 | |
| B. | 聚合物的链节是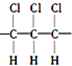 | |
| C. | 合成该聚合物的单体是CHCl═CHCl | |
| D. | 若n表示聚合度,则其相对分子质量为97n |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | a | |||||||
| 2 | b | c | d | |||||
| 3 | e | f | ||||||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高温下Mg2+得电子的能力比Rb+弱 | |
| B. | MgCl2对热的稳定性比RbCl强 | |
| C. | 在一定条件下,Mg的金属性比Rb强 | |
| D. | 铷的沸点比镁低,及时抽走铷蒸气使平衡向正反应方向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com