
焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
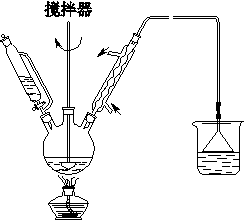
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2===Na2S2O5。
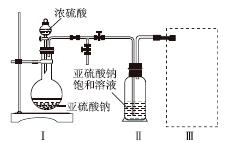
(1)装置Ⅰ中产生气体的化学方程式为______________________________________。
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是______。
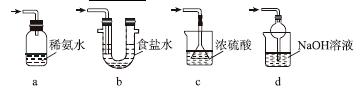
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为________(填序号)。
实验二 焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3。
(4)证明NaHSO3溶液中HSO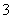 的电离程度大于水解程度,可采用的实验方法是________(填序号)。
的电离程度大于水解程度,可采用的实验方法是________(填序号)。
a.测定溶液的pH b.加入Ba(OH)2溶液
c.加入盐酸 d.加入品红溶液
e.用蓝色石蕊试纸检测
(5)检测Na2S2O5晶体在空气中已被氧化的实验方案是
________________________________________________________________________
________________________________________________________________________。
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:滴定时反应的化学方程式为SO2+I2+2H2O===H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为________g·L-1。
②在上述实验过程中,若有部分HI被空气氧化,则测定结果________(填“偏高”“偏低”或“不变”)。
(1)Na2SO3+H2SO4===Na2SO4+SO2↑+H2O(或Na2SO3+2H2SO4===2NaHSO4+SO2↑+H2O)
(2)过滤 (3)d (4)a、e
(5)取少量Na2S2O5晶体于试管中,加适量水溶解,滴加足量盐酸,振荡,再滴入氯化钡溶液,有白色沉淀生成 (6)①0.16 ②偏低
[解析] (1)据装置Ⅱ中所发生的反应可知:装置Ⅰ是制取SO2的发生装置,其化学方程式为Na2SO3 + H2SO4 === Na2SO4 + SO2↑+ H2O或者Na2SO3 + 2H2SO4===2NaHSO4 + SO2↑+ H2O。(2)析出的晶体要从溶液中获得可通过过滤的方法。(3)a中吸收尾气SO2的装置末端没有与大气相通,错误;b中该装置中SO2虽能与水反应且易溶于水,但还会有部分SO2进入空气,同时也会发生倒吸,错误;c中的浓硫酸不与SO2反应,错误;d中处理尾气SO2的同时也可起到防倒吸的作用,正确。(4)只要能证明NaHSO3溶液呈酸性的方法就可以,则选择a和e。(5)Na2S2O5中S元素的化合价为+4,若被氧气氧化则生成SO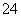 ,检验Na2S2O5晶体在空气中已被氧化的方案相当于检验硫酸根离子,则其实验方案是:取少量Na2S2O5晶体于试管中,加适量水溶解,滴加足量的盐酸振荡,再滴入氯化钡溶液,有白色沉淀生成。
,检验Na2S2O5晶体在空气中已被氧化的方案相当于检验硫酸根离子,则其实验方案是:取少量Na2S2O5晶体于试管中,加适量水溶解,滴加足量的盐酸振荡,再滴入氯化钡溶液,有白色沉淀生成。
(6) ①SO2 + 2H2O + I2===H2SO4 + 2HI
64 g 1 mol
x 0.01×25×10-3mol
求得:x=1.6×10-2g
则样品中抗氧化剂的残留量=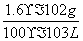 =0.16 g/L。
=0.16 g/L。
②. 若有部分HI被空气氧化生成I2,则所消耗标准I2溶液的体积减少,则测得样品中抗氧化剂的残留量将偏低。


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:
C6H12O6(葡萄糖)+Br2+H2O―→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7+CaCO3―→Ca(C6H12O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见下表:
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的 溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的 溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
实验流程如下:
C6H12O6溶液

 悬浊液
悬浊液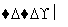
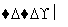
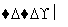 Ca(C6H12O7)2
Ca(C6H12O7)2
请回答下列问题:
(1)第①步中溴水氧化葡萄糖时,下列装置中最适合的是________。

A

B
C
制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其他试剂,下列物质中最适合的是________。
A.新制Cu(OH)2悬浊液
B.酸性KMnO4溶液
C.O2/葡萄糖氧化酶
D.[Ag(NH3)2]OH溶液
(2)第②步充分反应后CaCO3固体需有剩余,其目的是_____________________________;本实验中不宜用CaCl2替代CaCO3,理由是______________________________。
(3)第③步需趁热过滤,其原因是______________________________________________。
(4)第④步加入乙醇的作用是_________________________________________________。
(5)第⑥步中,下列洗涤剂最合适的是________。
A.冷水
B.热水
C.乙醇
D.乙醇水混合溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验可实现鉴别目的的是( )
A.用KOH溶液鉴别SO3(g)和SO2
B.用湿润碘化钾淀粉试纸鉴别Br2(g)和NO2
C.用CO2鉴别NaAlO2溶液和CH3COONa溶液
D.用BaCl2溶液鉴别AgNO3溶液和K2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验方案中,不能达到实验目的的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 检验CH3CH2Br在NaOH溶液中是否发生水解 | 将CH3CH2Br与NaOH溶液共热。冷却后,取出上层水溶液,用稀HNO3酸化,加入AgNO3溶液,观察是否产生淡黄色沉淀 |
| B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
| C | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到下层液体呈紫色 |
| D | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
磷酸铁(FePO4·2H2O,难溶于水的米白色固体)可用于生产药物、食品添加剂和锂离子电池的正极材料。实验室可通过下列实验制备磷酸铁。
(1)称取一定量已除去油污的废铁屑,加入稍过量的稀硫酸,加热、搅拌,反应一段时间后过滤。反应加热的目的是__________________________________。
(2)向滤液中加入一定量H2O2氧化Fe2+。为确定加入H2O2的量,需先用K2Cr2O7标准溶液滴定滤液中的Fe2+,离子方程式如下:
Cr2O +6Fe2++14H+===2Cr3++6Fe3++7H2O
+6Fe2++14H+===2Cr3++6Fe3++7H2O
①在向滴定管中注入K2Cr2O7标准溶液前,滴定管需要检漏、____________________和__________________。
②若滴定x mL滤液中的Fe2+,消耗a mol·L-1 K2Cr2O7标准溶液b mL,则滤液中c(Fe2+)=________mol·L-1。
③为使滤液中的Fe2+完全被H2O2氧化,下列实验条件控制正确的是________(填序号)。
A.加入适当过量的H2O2溶液
B.缓慢滴加H2O2溶液并搅拌
C.加热,使反应在较高温度下进行
D.用氨水调节溶液pH=7
(3)将一定量的Na2HPO4溶液(溶液显碱性)加入到含有Fe3+的溶液中,搅拌、过滤、洗涤、干燥得到FePO4·2H2O。若反应得到的FePO4·2H2O固体呈棕黄色,则磷酸铁中混有的杂质可能为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有K+、NH4+、Ba2+、SO42一、I一、 CO32一。分别取样:①用pH计测试,溶液显弱酸性;②加氯水和CCl4振荡后静置,下层呈无色。为确定该溶液的组成,还需检验的离子是 ( )
A.K+ B.SO42一 C.Ba2+ D.NH4+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com