
【题目】都能用下图所示装置进行喷泉实验的一组气体是

A.HCl和CO2B.NH3和CH4C.SO2和COD.NO2和NO
【答案】A
【解析】
只要充入的液体能使瓶内气体溶解或与之发生反应,且使瓶内气体处于低压状态,就可形成喷泉。
A. HCl极易溶于水,CO2 能完全溶于NaOH溶液中: 2NaOH+CO2 ═Na2CO3 +H2O或 NaOH+CO2 ═NaHCO3,能形成喷泉,故A选;
B. NH3 极易溶于水,可以形成喷泉,但CH4 难溶于水,也难溶于NaOH溶液,不能形成喷泉,故B不选;
C. SO2 能完全溶解在NaOH溶液中: 2NaOH+SO2 ══Na2 SO3 +H2 O或 NaOH+SO2 ══NaHSO3 ,可以形成喷泉,但CO不能溶解在NaOH溶液中,不能形成喷泉,故C不选;
D. NO2 能溶于NaOH溶液: 2NO2 +2NaOH══NaNO3 +NaNO2 +H2 O ,可以形成喷泉,但NO不能溶解在NaOH溶液中,不能形成喷泉,故D不选;
答案选A。


科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是原子序数依次递增的五种常见元素。A、B元素组成的气态化合物M的水溶液呈碱性,C元素是地壳中含量最多的元素,D的单质在C的单质中燃烧后的产物可以使品红溶液褪色,E是金属元素。
(1)写出A、C两种元素组成的化合物A2C2的电子式_______。
(2)若将E金属投入盐酸中,生成了浅绿色溶液N。则N的酸性溶液与A2C2反应的离子方程式为______________________________________。
(3)R是B的氧化物,通常情况下呈红棕色。现有一试管R,欲使元素B全部转化为它的最高价氧化物对应的水化物,故进行如下实验操作:将盛有R的试管倒扣在水槽中,______。
(4)有人设想寻求合适的催化剂和电极材料,以A2、B2为电极反应物,以HCl—NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极反应式_____________,放电时,溶液中的H+移向_________(填正极或负极)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示实验装置用于测定气体摩尔体积,相关叙述正确的是( )
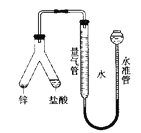
A. 用CCl4代替水,测得氢气的体积更准确
B. 量气管压入漏斗的水过多而溢出,会导致测定失败
C. 必须待体系温度降低到0℃时才可进行读数
D. 上提水准管,量气管液面高度不断改变,说明装置漏气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在“测定1mol气体体积”的实验中,我们通常选择的测量气体是氢气,反应是镁和稀硫酸反应。图中的A、B、C三部分能组成气体摩尔体积测定装置:
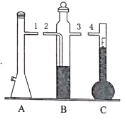
(1)C装置的名称是___________________。
(2)A、B、C装置接口的连续顺序是_________________。
(3)该装置正确连接后怎样做气密性检查?_________________。
(4)本实验中有两次针筒抽气,需要记录的是第____次抽出气体的体积。
(5)下表是某同学记录的实验数据:温度:25℃,气压:101.3kPa
实验次数 | 镁带质量(g) | 硫酸体积(mL) | C瓶读数(mL) | 抽出气体的体积(mL) |
1 | 0.115 | 10.0 | 124.8 | 7.0 |
2 | 0.110 | 10.0 | 120.7 | 6.2 |
计算两次实验1mol氢气的体积的平均值=____L(保留一位小数,镁的相对原子质量为24.3)。
(6)已知实验温度下,1mol氢气的体积的理论值为24.5L,实验误差=____%(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现将0.1mol某烃完全燃烧生成的气体全部依次通过浓硫酸和氢氧化钠溶液,经测定,前者增重10.8g,后者增重22g(假定气体全部吸收)。试通过计算推断该烃的分子式___(要有简单计算过程)并写出所有同分异构体___。若该烃的一氯代物只有一种,试写出该氯代烃的结构简式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了体育大型比赛的公平和发扬积极向上健康精神,禁止运动员使用兴奋剂是奥运会的重要举措之一。以下两种兴奋剂的结构分别为:
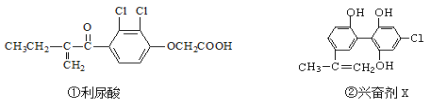
则关于以上两种兴奋剂的说法中正确的是( )
A. 利尿酸分子中有三种含氧官能团,在核磁共振氢谱上共有六个峰
B. 两种兴奋剂最多都能和含3molNaOH的溶液反应
C. 1 mol兴奋剂X与足量浓溴水反应,最多消耗4 mol Br2
D. 两种分子中的所有碳原子均不可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是四种常见有机物的比例模型示意图,下列说法正确的是
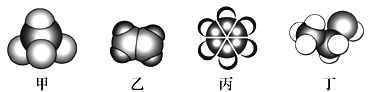
A. 甲能发生氧化反应
B. 乙通入溴的四氯化碳溶液,最后得到无色溶液不能和液溴反应
C. 煤干馏得到的煤焦油可以分离出丙,丙是无色无味的液态烃
D. 丁发生催化氧化得到的产物不能与金属钠反应
【答案】A
【解析】根据原子成键特点知,碳原子能形成4个共价键、H原子能形成1个共价键、O原子能形成2个共价键,根据分子比例模型及原子成键特点知,甲、乙、丙、丁分别是甲烷、乙烯、苯和乙醇;A.甲烷性质较稳定,不易被一般的强氧化剂氧化,但能在氧气中燃烧,发生氧化反应,故A正确;B.碳碳不饱和键能和溴发生加成反应,乙烯中含有碳碳双键,所以能和溴发生加成反应而使溴的四氯化碳溶液褪色,同时生成1,2-二溴乙烷,溶于CCl4,1,2-二溴乙烷在光照条件下能和液溴发生取代反应,故B错误;C.从煤焦油中可以获取苯,但苯有特殊的气味,故C错误;D.乙醇发生催化氧化得到的产物乙酸,有酸性,能与金属钠反应,故D错误;答案为A。
【题型】单选题
【结束】
23
【题目】某有机物A由C、H、O三种元素组成,相对分子质量为90。将9.0gA完全燃烧的产物依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g。A能与NaHCO3溶液发生反应,且2分子A之间脱水可生成六元环化合物。有关A的说法正确的是( )
A. 分子式是C3H8O3
B. A催化氧化的产物能发生银镜反应
C. 0.1molA与足量Na反应产生2.24L H2(标准状况)
D. A在一定条件下发生缩聚反应的产物是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列编号代表元素周期表中的一部分元素,用化学式或元素符号回答下列问题:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
一 | ||||||||
二 | ⑥ | ⑩ | ||||||
三 | ① | ③ | ⑤ | ⑦ | ⑨ | |||
四 | ② | ④ | ⑧ |
(1)①、③、⑤的最高价氧化物的水化物碱性最强的是_______(填化学式,下同)。
(2)②、③、④形成的简单阳离子半径由大到小的顺序是______________。
(3)①和⑧的最高价氧化物对应的水化物化学式为________和________。①和⑧两元素形成的化合物的化学式为________,该化合物的溶液与元素⑦的单质反应的离子方程式为_______________________。
(4)⑦、⑧、⑩三种元素形成的气态氢化物最稳定的是________(填化学式,下同),三种元素非金属性由强到弱的顺序为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产苯乙烯是利用乙苯的脱氢反应如下,针对上述反应,在其它条件不变时,下列说法正确的是( )

A. 加入适当催化剂,可以提高苯乙烯的产量
B. 在保持体积一定的条件下,充入较多的乙苯,可以提高乙苯的转化率
C. 仅从平衡移动的角度分析,工业生产苯乙烯选择恒压条件优于恒容条件
D. 加入乙苯至反应达到平衡过程中,混合气体的平均相对分子质量不断增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com