
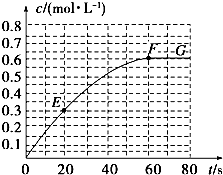
 298Kʱ��ij�ݻ��̶�Ϊ1L���ܱ������м���0.5mol A�������¿��淴Ӧ��A��g���T2B��g����H=a kJ?mol-1������B�����ʵ���Ũ����ʱ��仯��ͼ��
298Kʱ��ij�ݻ��̶�Ϊ1L���ܱ������м���0.5mol A�������¿��淴Ӧ��A��g���T2B��g����H=a kJ?mol-1������B�����ʵ���Ũ����ʱ��仯��ͼ��| 1 |
| 6 |
| ��c |
| ��t |
| 0.6mol/L |
| 60s |
| 1 |
| 2 |
| c2(B) |
| c(A) |
| c2(B) |
| c(A) |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ͭ���ڲ����ý�������ȴ�ܱ�FeCl3��Һ��ʴ����д�������ӷ�Ӧ����ʽ
ͭ���ڲ����ý�������ȴ�ܱ�FeCl3��Һ��ʴ����д�������ӷ�Ӧ����ʽ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� |
B�� |
C�� |
D�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ѡ�� | ʵ����� | ʵ������ | ���ͻ���� |
| A | ��S02ͨ����ɫʯ����Һ�� | ��ɫ��ȥ | SO2����Ư���� |
B | ��NaOH��Һ�еμ�������MgCl2��Һ�� Ȼ���ٵμ�������CuCl2��Һ | �Ȳ�����ɫ������Ȼ ���������ɫ | KSP[Cu��OH��2]��KSP[Mg��OH��2] |
| C | ��ij��Һ�еμ�KSCN��Һ | ��Һ���ɫ | ��Һ�к���Fe3+ |
| D | ������N02���ܱղ������������ˮ�� | ����ɫ���� | ��Ӧ2NO2��g��?N2O4��g���ġ�H��0 |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��16g | B��16 |
| C��32g | D��16g/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��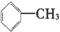 |
B�� |
C��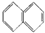 |
D��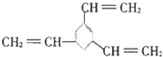 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com