
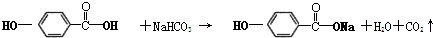 ,
, ,等物质的量B与Na、NaOH、NaHCO3充分反应,消耗Na、NaOH、NaHCO3的物质的量之比为3:2:1.
,等物质的量B与Na、NaOH、NaHCO3充分反应,消耗Na、NaOH、NaHCO3的物质的量之比为3:2:1.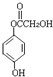 等(只写一种).
等(只写一种).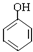 .
.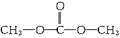 .
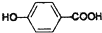
. 分析 (1)①A中羧基和酚羟基都能和NaOH发生中和反应,只有羧基能和碳酸氢钠反应生成二氧化碳,据此书写方程式;
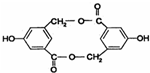
②有机物B在浓H2SO4存在下,相互作用生成一种环状酯,根据酯的结构简式知,B结构简式为 ,B中酚羟基、醇羟基和羧基都能和钠反应,酚羟基和羧基能和NaOH反应,只有羧基能和碳酸氢钠反应;
,B中酚羟基、醇羟基和羧基都能和钠反应,酚羟基和羧基能和NaOH反应,只有羧基能和碳酸氢钠反应;
③D与B为同分异构体,D不与NaHCO3反应,不含羧基,能与Na与NaOH反应,等质量D消耗Na、NaOH物质的量之比为2:3,含有1个羧酸与酚形成的酯基、1个酚羟基、1个醇羟基,D苯环上一氯取代物只有两种,应含有2个取代基且处于对位(或者含有2个酚羟基、1个醇与羧酸形成的酯基);
④等物质的量的A、C完全燃烧,消耗氧气的质量相等,且1molC能和1molNa完全反应,含有1个-OH或-COOH,将A的分子式改写C6H6O•CO2,则等物质的量的C6H6O与A耗氧量相等,故含碳原子数最少的C的结构简式为 ;
;
(2)分子式为C3H6O3的物质有多种同分异构体,
①因为1 mol甲(C3H6O3)与足量钠反应生成1 mol H2,则甲分子中含有两个-OH和一个-COOH,若甲与NaHCO3溶液反应,且分子中无甲基;若能发生银镜反应,则含有醛基;
②丙与金属Na不反应,丙中不含羟基,氢的化学环境相同,说明氢原子都是等效的;因为碳、氧各有两种不同的化学环境,说明丙分子中的碳原子、氧原子有两种不同位置.
解答 解:(1)①酚羟基与碳酸氢钠不反应,羧基与碳酸氢钠反应,最终生成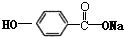 、二氧化碳与水,反应方程式为:
、二氧化碳与水,反应方程式为: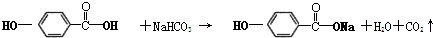 ,
,
故答案为: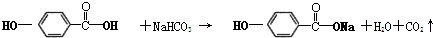 ;
;
②根据有机物B形成的环状酯类化合物(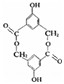 )可知,B为
)可知,B为 ,1molB含有2mol-OH、1mol-COOH,消耗Na3mol,1molB含有1mol酚羟基、1mol-COOH,消耗2mol氢氧化钠,1molB含有1mol-COOH,消耗1mol碳酸氢钠,故消耗Na、NaOH、NaHCO3的物质的量之比为3mol:2mol:1mol=3:2:1,
,1molB含有2mol-OH、1mol-COOH,消耗Na3mol,1molB含有1mol酚羟基、1mol-COOH,消耗2mol氢氧化钠,1molB含有1mol-COOH,消耗1mol碳酸氢钠,故消耗Na、NaOH、NaHCO3的物质的量之比为3mol:2mol:1mol=3:2:1,
故答案为:3:2:1;
③D与B为同分异构体,D不与NaHCO3反应,不含羧基,能与Na与NaOH反应,等质量D消耗Na、NaOH物质的量之比为2:3,含有1个羧酸与酚形成的酯基、1个酚羟基、1个醇羟基,D苯环上一氯取代物只有两种,应含有2个取代基且处于对位(或者含有2个酚羟基、1个醇与羧酸形成的酯基),则D的结构简式为: 等,故答案为:
等,故答案为: 等;
等;
④等物质的量的A、C完全燃烧,消耗氧气的质量相等,且1molC能和1molNa完全反应,C含有1个-OH或-COOH,将A的分子式改写C6H6O•CO2,则等物质的量的C6H6O与A耗氧量相等,故含碳原子数最少的C的结构简式为 ,
,
故答案为: ;
;
(2)①:因为1 mol甲(C3H6O3)与足量钠反应生成1 mol H2,则甲分子中含有两个-OH和一个-COOH.若甲与NaHCO3溶液反应,且分子中无甲基,故甲的结构简式CH2(OH)CH2COOH;若甲能发生银镜反应,则甲的结构简式为CH2(OH)CH(OH)CHO,故答案为:CH2(OH)CH2COOH;CH2(OH)CH(OH)CHO;
(3)丙中不含羟基,氢的化学环境相同,说明氢原子都是等效的;因为碳、氧各有两种不同的化学环境,说明丙分子中的碳原子、氧原子有两种不同位置,其结构简式为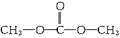 ,故答案为:
,故答案为: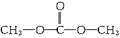 .
.
点评 本题考查有机物推断,侧重考查学生分析推断能力,根据物质的性质及官能团之间的关系推断物质,知道能分别和钠、NaOH、碳酸氢钠反应的官能团,题目难度不大.


科目:高中化学 来源: 题型:选择题
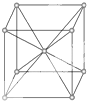
| A. | 是密置层的一种堆积方式 | B. | 晶胞是六棱柱 | ||
| C. | 每个晶胞内含2个原子 | D. | 每个晶胞内含6个原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酒石酸是有机二元酸 | B. | 酒石酸与铝盐性质相似 | ||
| C. | 酒石酸氢钾的溶解度小 | D. | 酒石酸钾的溶解度大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{c(N{H}_{3}•{H}_{2}O)}{c(O{H}^{+})}$ | B. | c(OH-) | C. | $\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$ | D. | c(NH4+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚钠中通二氧化碳反应:2C6H5O-+H2O+CO2→2C6H5OH+CO32- | |
| B. | 电解饱和食盐水:2H++2Cl?$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑ | |
| C. | Na2CO3溶液显碱性:CO32-+H2O═HCO3-+OH- | |
| D. | 足量AlCl3溶液与纯碱溶液混合:2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg>Al>Ca | B. | Al>Na>Li | C. | Al>Mg>Ca | D. | Mg>Ba>Al |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 氮是地球上极为丰富的元素.
氮是地球上极为丰富的元素.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com