
| A. | 甲烷 | B. | 乙烯 | C. | 苯 | D. | 二氧化硫 |
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:解答题
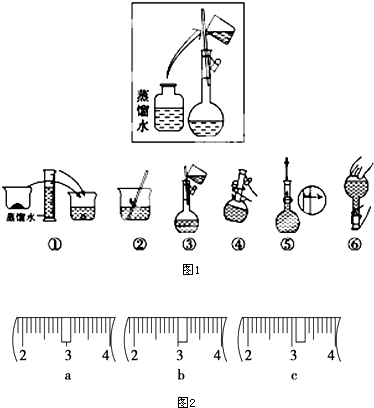 某同学帮助水质检测站配制230mL、1mol•L-1NaOH溶液以备使用.
某同学帮助水质检测站配制230mL、1mol•L-1NaOH溶液以备使用.| a | b | c | d | e | |
| 砝码大小/g | 100 | 50 | 20 | 10 | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| X(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| X(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
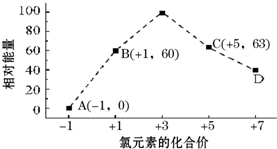 元素周期表中第ⅦA族元素的单质及其化合物的用途广泛.
元素周期表中第ⅦA族元素的单质及其化合物的用途广泛.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 线型结构的高分子材料分子间是靠分子间作用力紧密结合的,所以它的强度一定小 | |
| B. | 从实验测得的某高分子化合物的相对分子质量和小分子的相对分子质量含义不同 | |
| C. | 硫化橡胶为体型网状结构 | |
| D. | 线型结构的高分子,可带支链,也可不带支链 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 稀硫酸加入氢氧化钡溶液中:H++OH-═H2O | |
| B. | 铜片上滴加稀硝酸:3Cu+8H++2 NO3-═3Cu2++2NO↑+4H2O | |
| C. | 石灰石投入到稀醋酸中:CO32-+2 H+═CO2↑+H2O | |
| D. | Fe粉加入稀盐酸中:Fe+2H+═Fe2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
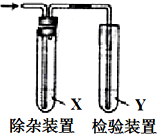 用如图所示装置检验气体时试剂X没必要或是错误的是( )
用如图所示装置检验气体时试剂X没必要或是错误的是( )| 检验的气体 | 试剂X | 试剂Y | |
| A | CH3CH2Br与NaOH乙醇溶液共热制备的乙烯 | H2O | Br2的CCl4溶液 |
| B | CH3CH2OH与浓H2SO4共热170℃制备的乙烯 | NaOH溶液 | 酸性KMnO4溶液 |
| C | 电石与饱和食盐水反应制备的乙烯 | 水 | 酸性KMnO4溶液 |
| D | 苯,液溴,铁屑混合反应生成的HBr | CCl4 | 硝酸银溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com