



科目:高中化学 来源: 题型:
| A、②③ | B、②④ | C、①② | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子数 | B、分子数 |
| C、质量 | D、密度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 氯化硼(BN)晶体是一种新型无机合成材料.用硼砂(Na2B4O7)和尿素反应可以得到氮化硼:Na2B4O7+2CO(NH2)2=4BN+Na2O+4H2O+2CO2↑
氯化硼(BN)晶体是一种新型无机合成材料.用硼砂(Na2B4O7)和尿素反应可以得到氮化硼:Na2B4O7+2CO(NH2)2=4BN+Na2O+4H2O+2CO2↑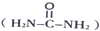 )中π键与σ键数目之比为
)中π键与σ键数目之比为查看答案和解析>>
科目:高中化学 来源: 题型:
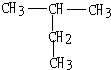 的系统名称为
的系统名称为 的命名为
的命名为查看答案和解析>>
科目:高中化学 来源: 题型:
| a | |||||||
| d | f | g | |||||
| b | c | e | h | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com