
SO2�����ŷŻ�������صĴ�����Ⱦ��������ijС��ͬѧ��ƴ�����������Ҫ��SO2��N2��O2���۳�����SO2�ķ�����
��1������һ�������ȼҵ��Ʒ����SO2���������������£�
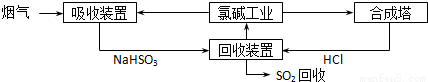
�١�����װ�á��з�����Ӧ�����ӷ���ʽ_____________________��
�ںϳ�����ÿ�ϳ�1mol����ų�����92.3kJ��25�桢101kPa������Ӧ���Ȼ�ѧ����ʽ_____________��
������������ѭ�����õ�������____________________��
��2��������������FeCl3��Һ��������������SO2
�ٸ÷�Ӧ�����ӷ���ʽ________________________����Ӧa����Ϊ��֤�÷�Ӧ��ͬѧ�ǽ�SO2ͨ��0.05mol/LFeCl3��Һ�У���Һ�ܿ��� ��ɫ��Ϊ���ɫ������Һ��ʱ����ú����ձ�
��ɫ��Ϊ���ɫ������Һ��ʱ����ú����ձ� Ϊdz��ɫ�����ں��ɫҺ�壬������ͬѧ�ǵķ����Ʋ�
Ϊdz��ɫ�����ں��ɫҺ�壬������ͬѧ�ǵķ����Ʋ� ��
�� ʵ�顣
ʵ�顣
�����Ʋ� | ʵ�鲽�輰���� |
�ף�������Fe(OH)3���� �ң� Fe3++6SO2 | I���Ʊ�Fe(OH)3���岢���� II���ֱ���Fe(OH)3����ú��ɫҺ���м����������ۣ���ǰ�߲���ɫ�����߱�Ϊdz��ɫ |
�����ý����_________________�������ʣ����Լ��鲽��I���Ƿ�õ���Fe(OH)3���塣
�۸��ݷ�Ӧb˵������II��Һ����ɫ�仯��ԭ����______________________�������ӷ���ʽ����Ҫ������˵������
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ��������У��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ǿ�����ɫ��Һ�У����и��������ܴ����������( )
A�� K+��Na+��NO3-��Br- B��Na+��NH4+��NO3-��Cl-
C��K+��Na+��HCO3- ��NO3- D��K+��Cu2+��Cl-��SO42-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ�Ϻӿ��и���10���¿���ѧ���������棩 ���ͣ�ѡ����
�� 4 mol A ����� 2 mol B ������ 2 L �������л�ϲ���һ�������·������·�Ӧ��2A������ �� B������  2C���������� 2 s���룩���� C ��Ũ��Ϊ 0.6 mol��L��1 ���������м���˵������ ������ A ��ʾ�ķ�Ӧ��ƽ������Ϊ 0.3 mol��L��1��s��1 �� ������ B ��ʾ�ķ�Ӧ��ƽ������Ϊ 0��6 mol��L��1��s��1 ��2 s ʱ���� B ��Ũ��Ϊ 0.7 mol��L��1 ��2 s ʱ���� A ��ת����Ϊ70�� ������ȷ���ǣ� ��
2C���������� 2 s���룩���� C ��Ũ��Ϊ 0.6 mol��L��1 ���������м���˵������ ������ A ��ʾ�ķ�Ӧ��ƽ������Ϊ 0.3 mol��L��1��s��1 �� ������ B ��ʾ�ķ�Ӧ��ƽ������Ϊ 0��6 mol��L��1��s��1 ��2 s ʱ���� B ��Ũ��Ϊ 0.7 mol��L��1 ��2 s ʱ���� A ��ת����Ϊ70�� ������ȷ���ǣ� ��
A���٢� B���٢� C���ڢ� D���ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ�Ϻӿ��и���10���¿���ѧ���������棩 ���ͣ�ѡ����
�����£�ij��ɫ��Һ��������Ӧ�ų�����������Һ��һ���ܴ������ڵ��������ǣ��� ��
A�� Na+��Cl����K+��SO42��  B��Mg2+��NH4+��SO42����Cl��
B��Mg2+��NH4+��SO42����Cl��
C�� Na+��K+��MnO4����SO42�� D��Na+��K+��CO32����NO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ�Ϻӿ��и���10���¿���ѧ���������棩 ���ͣ�ѡ����
��98%��ŨH2SO4(�ܶ�Ϊ1.84g/cm3)����1 mol/L��ϡH2SO4 90 mL�����ƹ����������������Ⱥ�˳����( )
��20 mL��Ͳ ��10 mL��Ͳ ��50 mL�ձ� ��������ƽ ��100 mL����ƿ ��ͷ�ι� �߲�����
A���٢ۢݢޢ� B���ڢۢߢݢ�
C���ڢݢߢޢ� D���ܢۢߢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017����������и���������11���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ�������£�X��ǿ�ᡢǿ����Һ��Ӧ���£�������˵����ȷ���ǣ� ��
Y X
X Z��
Z��
A����XΪ����������Y���������ֻ��������
B����XΪNaHCO3����Zһ����CO2
C����Y��ZΪ����Ԫ�ص������Σ���Xһ��ΪAl��OH��3
D����XΪ������������������Y��Z�о������Ҵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�츣��ʡ����������һ��ѧ���������棩 ���ͣ������
�Ȼ��Ⱦ����ڹ�ҵ�ϳ��������Ļ�ʴ������ҵ��һ����������ˮ�ĵ�̼���ȣ�SrCO3��Ϊԭ�ϣ��������������Ļ�����ȣ����Ʊ��ߴ���ˮ�Ȼ��Ⱦ��壨SrCl2•6H2O���Ĺ���Ϊ��

��֪����SrCl2•6H2O������61��ʱ��ʼʧȥ�ᾧˮ��100��ʱʧȥȫ���ᾧˮ��
���й��������↑ʼ��������ȫ������pH���±���
�������� | Fe(OH)3 | Fe(OH)2 |
��ʼ������pH | 1.5 | 6.5 |
������ȫ��pH | 3.7 | 9.7 |
��1���������� ʵ�ʹ�ҵ�����г�����̼���ȷ��鲢���Խ��裬��Ŀ���� ��̼���������ᷴӦ�Ļ�ѧ����ʽΪ__________________��
ʵ�ʹ�ҵ�����г�����̼���ȷ��鲢���Խ��裬��Ŀ���� ��̼���������ᷴӦ�Ļ�ѧ����ʽΪ__________________��
��2���������� ���������£�����30% H2O2��Һ��Ŀ���ǣ� ��
���������£�����30% H2O2��Һ��Ŀ���ǣ� ��
��3�������۽���Һ��pHֵ��1������ ����ѡ���������������Ҫ�ɷ��� ���ѧ ʽ����
ʽ����
A��1.5 B��4 C��7 D��9.7
��4����ҵ����50��60���ȷ紵����ˮ�Ȼ��ȣ�ѡ����¶ȵ�ԭ���� ��
��5���������У�ϴ���Ȼ��Ⱦ������ѡ��___________��
A��ˮ B��ϡ���� C������������Һ D���Ȼ��ȱ�����Һ
��6������Һ��Ba2+ Ũ��Ϊ1��10��5mol/L������Һ��Sr2�����ʵ���Ũ�Ȳ����� mol/L��
����֪��Ksp[SrSO4]=3.3��10��7��Ksp[BaSO4]=1.1��10��10��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�찲��ʡ��У�����о�������ϵ�һ��������ѧ���������棩 ���ͣ������
ij�����û��շ�������VOSO4��K2SO4��SiO2��)��ȡV2O5ʱ�����������£�
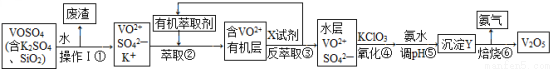
��ش��������⣺
��1������I������ �����в�����������Ҫ�ɷ��� ��
��2����֪��VOSO4��ˮ�㣩+2HA���л��㣩 VOA2���л��㣩+H2SO4��ˮ�㣩��������б�������������ԭ���� ��������з���ȡ���õ��Լ�XΪ ��
VOA2���л��㣩+H2SO4��ˮ�㣩��������б�������������ԭ���� ��������з���ȡ���õ��Լ�XΪ ��
��3��������еķ�Ӧ�����ӷ���ʽ����ClO3��+��VO2++��H+����VO3++�� +��
��4������Y��Ħ������Ϊ598g��mol��1���ҽ���������Ԫ�ء�ȡ59.8g����Y����Ʒ��ֱ��գ��õ���Ʒ54.6g��������������ͨ��������ʯ�ң���ʯ������1.8g��ʣ���������ͨ��ϡ���ᱻ��ȫ���ա�ͨ������ȷ������Y�Ļ�ѧʽΪ ��
��5���������ʺ���ҺpH֮���ϵ����
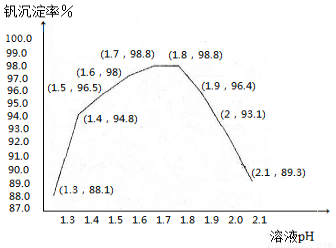
���м��백ˮ��������Һ�����pHΪ ������������Ϊ93.1%ʱ������Fe(OH)3����������Һ��c(Fe3+)�� ������֪��25��ʱ��Ksp[Fe(OH)3]��2.6��l0��39)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�찲��ʡ����ʮУ����11���ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
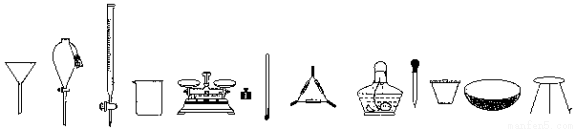
a b c d e f g h I j k l
A. ��ɰ����ʳ��ˮ���ˣ�ѡ��a��d��f��l
B. ��ȡˮ�е⣬ѡ��b��c��d��f
C. ������ת��ΪCuSO4���壬ѡ��g��h��j��l
D. ������Һ�е�Fe3+��ѡ��d��f��h��i
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com