
分析 根据题目信息可知:用CO还原MgSO4,750℃时可得到MgO、SO2和SO3,且含等物质的量SO2和SO3,硫的化合价降低,根据得失电子守恒和原子守恒还有CO2生成,再根据质量守恒配平.
解答 解:750℃时,用CO还原MgSO4可得到MgO、等物质的量SO2和SO3,硫的化合价降低,镁化合价不变,则碳元素化合价升高,所以必有CO2生成,S(+6→+4),C(+2→+4),所以二氧化硫与二氧化碳系数比为1:1,根据质量守恒方程式为CO+2MgSO4 $\frac{\underline{\;高温\;}}{\;}$2MgO+CO2+SO2+SO3,
故答案为:CO+2MgSO4 $\frac{\underline{\;高温\;}}{\;}$2MgO+CO2+SO2+SO3.
点评 本题考查方程式的书写,根据题干信息结合氧化还原知识是解答关键,题目难度不大.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:选择题
| A. | “可燃冰”有可能成为人类未来的重要能源 | |
| B. | “可燃冰”是一种比较洁净的能源 | |
| C. | “可燃冰”提供了水可能变成油的例证 | |
| D. | “可燃冰”的主要可燃成分是甲烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 和
和 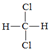 ④CH3CH2CH3和CH3CH3 ⑤氕和氘 ⑥CH3CH2CH2CH2CH3和CH3C(CH3)3
④CH3CH2CH3和CH3CH3 ⑤氕和氘 ⑥CH3CH2CH2CH2CH3和CH3C(CH3)3查看答案和解析>>
科目:高中化学 来源: 题型:解答题
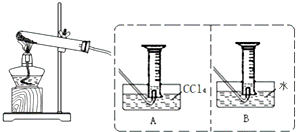
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 实验操作 | 实验目的 |
| A | Cl2、Br2分别与H2反应 | 比较氯、溴的非金属性强弱 |
| B | 向MgCl2、AlCl3溶液中分别通入NH3 | 比较镁、铝金属性强弱 |
| C | 测定相同物质的量浓度的Na2CO3、Na2SO4溶液的pH | 比较碳、硫的非金属性强弱 |
| D | Fe、Cu分别与稀盐酸反应 | 比较铁、铜的金属性强弱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
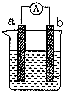 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:
如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com