
【题目】将2 mol N2(g)和1 mol H2(g)置于2L密闭容器中,在一定温度下发生反应:N2(g)+3H2(g)![]() 2NH3(g) H<0,其他条件不变时,改变某一条件对上述反应的影响,得出下列关系图:
2NH3(g) H<0,其他条件不变时,改变某一条件对上述反应的影响,得出下列关系图:
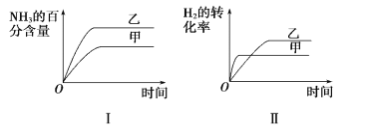

下列说法正确的是
A.图Ⅰ研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
B.图Ⅱ研究的是压强对反应的影响,且乙的压强较高
C.图Ⅱ研究的是温度对反应的影响,且乙的温度较高
D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高
【答案】D
【解析】
A.催化剂只能改变反应速率,缩短达到平衡所需要的时间,不能使化学平衡发生移动,因此图Ⅰ研究的是不是催化剂的影响,A错误;
B.在其它条件不变时,增大压强,化学反应速率加快,达到平衡所需要的时间缩短,所以应该甲的压强较高;另外,如果研究的是压强的影响,增大压强,平衡向正反应方向移动,氢气的转化率应该增大,和图像不符,B错误;
C.温度升高,反应速率加快,达到平衡所需要的时间缩短,所以温度甲>乙,升高温度,平衡向吸热的逆反应方向移动,达到平衡时,H2转化率降低,图Ⅱ研究的不是是温度对反应的影响,C错误;
D.催化剂能够加快反应速率,缩短达到平衡所需要的时间,而不能使化学平衡发生移动,因此混合物中各组分的含量不变,总物质的量也不变,故图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高,D正确;
故合理选项是D。


 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:
【题目】反应N2+3H2 ![]() 2NH3刚开始时,N2的浓度为3mol·L-1 ,H2的浓度为5mol·L-1,3min后测得NH3的浓度为0.6mol·L-1则此时间内,下列反应速率表示正确的是( )
2NH3刚开始时,N2的浓度为3mol·L-1 ,H2的浓度为5mol·L-1,3min后测得NH3的浓度为0.6mol·L-1则此时间内,下列反应速率表示正确的是( )
A.v (NH3)= 0.1 mol˙L-1˙min-1B.v (N2) = 1.0 mol˙L-1˙min-1
C.v (H2) = 1.67 mol˙L-1˙min-1D.v (H2) = 0.3 mol˙L-1˙min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将100 mL 1 mol·L-1的氨水与100 mL a mol·L-1盐酸等体积混合,忽略反应放热和体积变化,下列有关推论不正确的是
A. 若混合后溶液pH=7,则c(NH4+)=c(Cl-)
B. 若a=2,则c(Cl-)>c(NH4+)>c(H+)>c(OH-)
C. 若a=0.5,则c(NH4+)>c(Cl-)>c(OH-)>c(H+)
D. 若混合后溶液满足c(H+)=c(OH-)+c(NH3·H2O),则可推出a=1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知乙烯能发生以下转化:

(1)A的名称为_____________;
(2)①的反应方程式___________________;①的反应类型___________;
(3)②的反应方程式_____________;②的反应类型是__________________;
(4)浓H2SO4的作用_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1 L密闭容器中,发生反应N2(g)+3H2(g)![]() 2NH3(g),若最初加入的N2和H2物质的量均为4 mol,测得10s内H2的平均速率v(H2)=0.12 molL-1s-1,则反应进行到10s时容器中N2的物质的量是
2NH3(g),若最初加入的N2和H2物质的量均为4 mol,测得10s内H2的平均速率v(H2)=0.12 molL-1s-1,则反应进行到10s时容器中N2的物质的量是
A.1.6molB.2.8molC.3.2molD.3.6mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究黑色固体 X(仅含两种元素)的组成和性质,设计并完成如下实验:
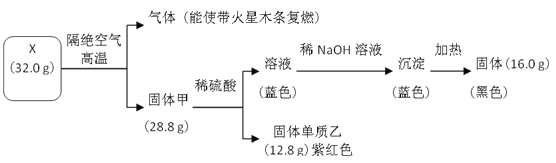
请回答:
(1)X 的化学式是______________。
(2)写出蓝色溶液转化为蓝色沉淀的离子方程式是______________。
(3)写出固体甲与稀硫酸反应的化学方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应CCl4 +4Na![]() C(金刚石)+4NaCl可实现人工合成金刚石。下列关于该反应的说法错误的是( )
C(金刚石)+4NaCl可实现人工合成金刚石。下列关于该反应的说法错误的是( )
A.C(金刚石)属于原子晶体
B.该反应利用了Na的强还原性
C.CCl4和C(金刚石)中的C的杂化方式相同
D.NaCl晶体中每个Cl-周围有8个Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25°C时,向10mL0.10mol·L-1的一元弱酸HA(Ka =1.0×10-3)中逐滴加入0.10mol·L-1NaOH溶液,溶液pH随加入NaOH溶液体积的变化关系如图所示。下列说法正确的是( )
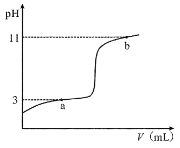
A.a点时,c(HA)+c(OH-)=c(Na+)+c(H+)
B.溶液在a点和b点时水的电离程度相同
C.b点时,c(Na+)=c(HA)+c(A- )+c(OH-)
D.V =10mL时,c(Na+)>c(A-)>c(H+)>c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50 mL 0.5 mol/L的盐酸与50 mL 0.5 mol/L的NaOH 溶液在下图所示的装置中进行中和热测定实验,下列说法不正确的是
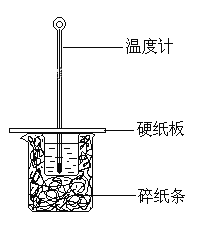
A.图中实验装置缺少环形玻璃搅拌棒,烧杯间填满碎纸条的主要作用是固定小烧杯
B.稀溶液中:H+ (aq) + OH— (aq) = H2O (l) ΔH=-57.3kJ·mol-1 ,若将含0.5 mol H2SO4的稀溶液与含1 mol NaOH的稀溶液混合,放出的热量为57.3kJ
C.进行中和热测定实验时,需要测出反应前盐酸和NaOH溶液的温度及反应后溶液的最高温度
D.若改用55 mL 0.50 mol/L的盐酸跟50 mL0.5 mol/L的NaOH溶液进行实验,从理论上说所求中和热相等。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com