
| c(标准)×V(标准) |
| V(待测) |
| c(标准)×V(标准) |
| V(待测) |
| 5 |
| 2 |
| 0.100mol/L×24.20mL |
| 25.00mL |


 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
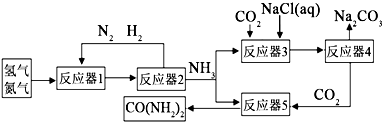
| ||
| 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④ | B、②③ |
| C、②⑦ | D、④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
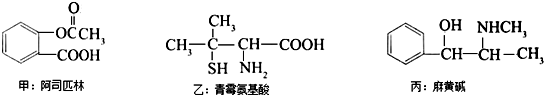
| A、都能发生酯化反应 |
| B、都能与NaOH反应 |
| C、甲的苯环上的一氯代物有4种 |
| D、丙的分子式为C10H15ON,苯环上的一氯代物有3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若生成1 molP(g),则放出的热量等于a kJ |
| B、若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| C、若升高温度,正反应速率加快,逆反应速率减慢,化学平衡正向移动 |
| D、达到化学平衡状态时,若c(Y)=0.100mol/L,则c(P)=0.0203 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
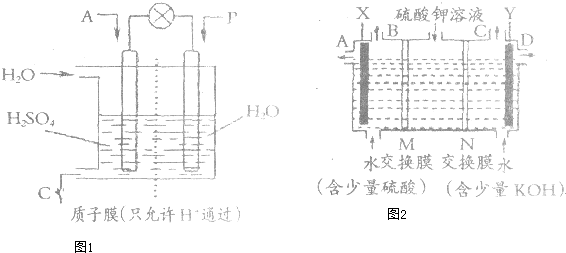
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
| 3%溴水 |
| 55℃ |
| 过量CaCO3 |
| 70℃ |
| 趁热过滤 |
| 乙醇 |
| 过滤 |
| 洗涤 |
| 干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰 |
| B、小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂 |
| C、节日燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 |
| D、青铜是我国使用最早的合金材料,目前世界上使用量最大的合金材料是钢铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、便于运输、储存,从安全角度考虑,硅是最佳的燃料 |
| B、自然界的含硅化合物易开采 |
| C、硅燃烧放出的热量大,燃烧产物对环境污染程度低且容易有效控制 |
| D、自然界中存在大量单质硅 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com