
| A. | 合成氨技术实现了“从空气到面包” | |
| B. | 合成氨涉及氧化还原反应 | |
| C. | 高效催化剂是合成氨反应的重要条件 | |
| D. | 合成氨所需要的氢气主要来自于电解水 |
分析 A.合成氨的原料气中有氮气,通过化学变化得到氮肥可分析;
B.根据合成氨的化学方程式可分析出有化合价的升降,是氧化还原反应;
C.解决合成氨的关键在于要又快又多的得到氨气,采取高温高压、催化剂进行合成;
D.电解水的成本太高.
解答 解:A.合成氨的原料气中有氮气,通过化学变化:氮气→氨气→一氧化氮→二氧化氮→硝酸→硝酸盐、铵盐→肥料,粮食增产,所以合成氨技术实现了“从空气到面包”的说法是有道理的,故A正确;
B.合成氨的化学方程式:N2+3H2 $?_{催化剂}^{高温高压}$ 2NH3,氮的化合价降低,氢的化合价升高,是一个氧化还原反应,故B正确;
C.解决合成氨的关键在于要又快又多的得到氨气,采取高温高压、催化剂进行合成,所以高效催化剂是合成氨反应的重要条件,故C正确;
D.合成氨所需要的氢气主要来自于天然气、石脑油、重质油、煤、焦炭、焦炉气,电解水的成本太高,故D错误;
故选D.
点评 本题考查合成氨的价值,化学与生活的联系,合成氨的条件以及原料的选取,氧化还原反应的判断,都是基础知识.


科目:高中化学 来源: 题型:选择题
| A. | SO2是很好的抑菌剂,红酒中常加人微量的SO2 | |
| B. | 麦片中常加人微量铁粉,可以防止被氧化而变质 | |
| C. | “PM2.5“是指大气中直径≤2.5微米的颗粒物.其悬浮在空气中一定形成气溶胶 | |
| D. | 制饭勺、饭盒、高压锅等的不锈钢是合金 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
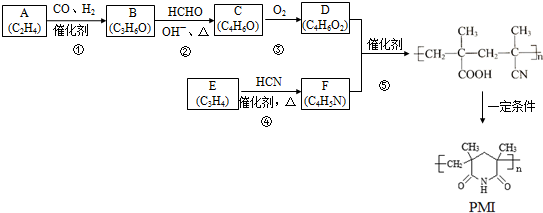
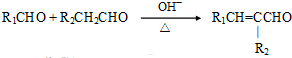 (注:R1可以是烃基本,也可以是H原子)
(注:R1可以是烃基本,也可以是H原子)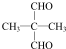 .
.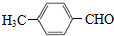 及其他物质为原料经如下步骤可合成对甲基苯丙烯酸甲酯:
及其他物质为原料经如下步骤可合成对甲基苯丙烯酸甲酯: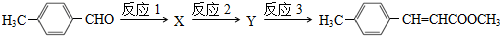
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
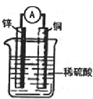 如图为某原电池示意图,请回答下列问题,
如图为某原电池示意图,请回答下列问题,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀释pH=3的醋酸,溶液中所有离子的浓度均降低 | |
| B. | 相同条件下,pH=5的①NH4C1溶液、②CH3C00H溶液、③稀盐酸溶液中由水电离出的c(H+):①>②>③ | |
| C. | 体积相同、浓度均为0.1mol/L的盐酸和醋酸,分别稀释m倍、n倍,溶液的pH都变成5,则m<n | |
| D. | pH=5的硫酸溶液稀释到原来的500倍,稀释后溶液中的c(SO42-)与c(H+)之比约为1:10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:F->Na+>Mg2+>Al3+ | B. | 热稳定性:HCl<H2S<PH3 | ||
| C. | 酸性:H2SiO3>H2CO3>H3PO4 | D. | 熔点:NaCl>SiO2>CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑦ | B. | ②⑤⑧ | C. | ③⑥⑨ | D. | 全部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com