
| A.用25mL量筒量取18.63mL盐酸 |
| B.用托盘天平称取12.15克食盐 |
| C.标准的NaOH溶液滴定未知浓度的盐酸,用去NaOH溶液32.30mL |
| D.用广泛pH试纸(1~14)测得某溶液pH为5.5 |
科目:高中化学 来源:不详 题型:单选题
| A.容量瓶用蒸馏水洗净后,再用待配液润洗 |
| B.使用容量瓶前检查它是否漏水 |
| C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近刻度线2-3cm处,用滴管滴加蒸馏水到刻度线 |
| D.配制溶液时,如果试样是液体,用量筒量取试样后直接到入容量瓶中,缓慢加入蒸馏水到接近刻度线2-3cm处,用滴管加蒸馏水到刻度线 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.洒水降温并溶解汽油蒸气 |
| B.开灯查找漏油部位,及时修理 |
| C.打开车窗,严禁烟火,疏散乘客离开车厢 |
| D.让车内人员坐好,不要随意走动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

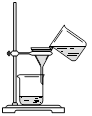

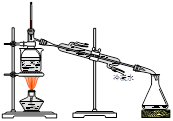
| A.将海带灼烧成灰 | B.过滤得合I—溶液 | C.放出碘的苯溶液 | D.分离碘并回收苯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.点燃氢气前要检验纯度,以免发生爆炸 |
| B.不慎将浓盐酸溅到皮肤上,要立即用浓碱溶液冲洗 |
| C.CO气体有毒,处理CO尾气的方法一般是将其点燃,转化成无毒的CO2 |
| D.在盛O2的集气瓶中进行铁丝燃烧实验时,事先在集气瓶底部铺上一层沙子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

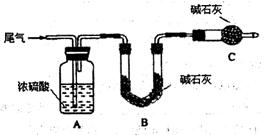
 6H2O晶体的操作包括 、冷却结晶、过滤,该过程需保持盐酸过量,结合必要的离子方程式说明原因 .
6H2O晶体的操作包括 、冷却结晶、过滤,该过程需保持盐酸过量,结合必要的离子方程式说明原因 .查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.锥形瓶可用作加热的反应器 |
| B.室温下,不能将浓硫酸盛放在铁桶中 |
| C.配制溶液定容时,俯视容量瓶刻度会使溶液浓度偏高 |
| D.用蒸馏水润湿的试纸测溶液的pH,一定会使结果偏低 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 实验目的或结论 |
| A | 将混有Ca(OH)2杂质的Mg(OH)2样品,放入水中搅拌成浆状后,加入足量饱和氯化镁溶液充分搅拌、过滤,沉淀用蒸馏水洗涤。 | 除去Mg(OH)2样品中的Ca(OH)2 |
| B | 取少量KClO3晶体溶于适量的蒸馏水,再加入硝酸 酸化的AgNO3溶液。 | 检验KC1O3中的氯元素 |
| C | 向某溶液中滴加Ba(NO3)2溶液产生白色沉淀,再加稀盐酸沉淀消失。 | 说明原溶液中一定含有CO32-或SO32- |
| D | 向盛有1mL 0.01lmol·L-1AgNO3溶液的试管中滴加5滴0.0lmol·L-1NaCl溶液,有白色沉淀生成,再向其中滴加0.01 mol·L-1 NaI溶液,产生黄色沉淀。 | 常温下, Ksp(AgCl)>Ksp(AgI) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com