
(08年北京卷) 下列叙述正确的是 ( )
A.将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO![]() )>c(NH
)>c(NH![]() )
)
B.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2
C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D.向0.1 mol/L的氨水中加入少量硫酸铵固体,则溶液中 增大
增大
答案:C
解析:A、根据溶液中电荷守恒知:c(H+)+c(NH4+)=2c(SO42-)+c(OH-),当溶液pH=7时,
c(H+)= c(OH-),那么有:c(NH4+)=2c(SO42-) 则A不正确;B、醋酸是弱酸,不同浓度的醋酸其电离程度不同,当pH相差一个单位时,c1>10c2 B不正确;C、.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合时,醋酸过量,溶液显酸性,滴入石蕊溶液呈红色,C正确;
D、向0.1 mol/L的氨水中加入少量硫酸铵固体,氨水的电离平衡向逆方向移动,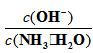 减少。
减少。
高考考点:溶液中离子浓度比较、弱电解质电离平衡及其移动
易错提醒:不能正确理解弱电解质电离的平衡的存在,造成BCD项错误判断
备考提示:解答离子浓度大小比较试题,抓住一个原理、两类平衡、三种守恒进行分析,包括化学平衡移动原理,电离平衡和水解平衡,电荷守恒、物料守恒和质子守恒。其中电荷守恒是指溶液中阳离子所带正电荷总数等于阴离子所带负电荷总数,溶液电中性; 物料守恒是指某一组分的原始浓度应该等于它在溶液中各种存在形式的浓度之和;质子守恒是指溶液中由水电离出来的H+和OH-总是相等的。质子守恒可由电荷守恒和物料守恒联立推导出来。


科目:高中化学 来源: 题型:
 (08年北京卷)(17分)X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核。通常状况下,W为无色液体。
(08年北京卷)(17分)X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核。通常状况下,W为无色液体。
已知:X+Y![]() Z+W
Z+W
(1)Y的电子式是_______________。
(2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是___。
(3)用图示装置制备NO并验证其还原性。有下列主要操作:
a.向广口瓶内注入足量热NaOH溶液,将盛有铜片的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入少量稀硝酸。
①步骤c后还缺少的一步主要操作是______________________。
②红磷充分燃烧的产物与NaOH溶液反应的离子方程式是_________。
③步骤c滴入稀硝酸后烧杯中的现象是______________
反应的离子方程式是_____________________________。
 (4)一定温度下,将1 mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。温度由T1继续升高到T2的过程中,气体逐渐变为无色。若保持T2,增大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图所示。
(4)一定温度下,将1 mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。温度由T1继续升高到T2的过程中,气体逐渐变为无色。若保持T2,增大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图所示。
①温度在T1-T2之间,反应的化学方程式是_________。
②温度在T2-T3之间,气体的平均相对分子质量是(保留1位小数)______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
A.分子中碳原子不在一条直线上
B.光照下能够发生取代反应
C.比丁烷更易液化
D.是石油分馏的一种产品
查看答案和解析>>
科目:高中化学 来源: 题型:
(08年山东卷)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g)===CH4(g)+HC≡CH(g)+H2(g);△H1=156.6 kJ?mol-1
CH3CH=CH2(g)===CH4(g)+HC=CH(g);△H2=32.4 kJ?mol-1
则相同条件下,反应C3H8(g)===CH3CH=CH2(g)+H2(g)的△H=_____kJ?mol-1
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应方程式为___________;放电时,CO32-移向电池的_______(填“正”或“负”)极。
(3)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol?L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3![]() HCO3- +H+的平衡常数K1=_____________。(已知:10-5.60=2.5×10-6)
HCO3- +H+的平衡常数K1=_____________。(已知:10-5.60=2.5×10-6)
(4)常温下,则溶液c(H2CO3)______c(CO32-)(填“>”、“=”或“<”),原因是_______________________(用离子方程式和必要的文字说明)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(08年北京卷)(13分)通常状况下,X、Y和Z是三种气态单质。X的组成元素是第三周期原子半径最小的元素(稀有气体元素除外);Y和Z均由元素R组成,反应Y+2I+2H+![]() I2+Z+H2O常作为Y的鉴定反应。
I2+Z+H2O常作为Y的鉴定反应。
⑴Y与Z的关系是(选填字母) 。
a.同位素 b.同系物 c.同素异形体 d.同分异构体
⑵将Y和二氧化硫分别通入品红溶液,都能使品红褪色。简述用褪色的溶液区别二者的实验方法 。
⑶举出实例说明X的氧化性比硫单质的氧化性强(用化学方程式表示)。
。
⑷气体(CN)2与X化学性质相似,也能与H2反应生成HCN(其水溶液是一种酸)。
①HCN分子中含有4个共价键,其结构式是 。
②KCN溶液显碱性,原因是(用离子方程式表示) 。
⑸加热条件下,足量的Z与某金属M的盐MCR3(C为碳元素)完全反应生成CR2和MmRn(m、n均为正整数)。若CR2质量为w1g,MmRn质量为w2g,M的相对原子质量为a,则MmRn中m:n= (用含w1、w2和a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(04年北京卷)在一定温度下,一定体积的密闭容器中有如下平衡:
![]()
已知H2和I2的起始浓度均为![]() 时,达平衡时HI的浓度为
时,达平衡时HI的浓度为![]() 。若H2和I2的起始浓度均变为
。若H2和I2的起始浓度均变为![]() ,则平衡时H2的浓度(
,则平衡时H2的浓度(![]() )是()
)是()
A. 0.16 B. 0.08 C. 0.04 D. 0.02
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com