
以下四组装置在下列实验可供选择

Ⅰ.实验室用甲醇催化氧化法得到甲醛,并验证甲醛的性质。请回答下列问题:
(1)应选择的装置是___ _____(填写编号)。
(2)若③硬质玻璃管中装有铜粉,请写出硬质玻璃管中发生反应的化学方程式__
_ __。
(3)实验结束后,观察到溴水褪色。为解释这一现象,某学习小组的同学提出两种猜想:
A. 发生了加成反应; B. 发生了氧化反应。
为探究哪种猜想正确,学习小组的同学用pH计测溴水褪色前后溶液的pH,测得溶液的pH下降,你认为发生何种反应,请说出你的理由
________________ ________________________________________________________。
Ⅱ.若选择①③②验证乙烯与氢气反应产物,请回答下列问题:
(4)写出实验室制乙烯的化学方程式_______________________________________。
(5)NaOH溶液的作用是(答两点即可)_____________________________________
_ _。
(6)实验过程中,发现③中溴水褪色,试用化学方程式表示溴水褪色的原因_______________ _ ___;
(7)出现什么现象可说明乙烯与氢气反应生成了乙烷
________________________________________________________________________。
【知识点】制备实验方案的设计;乙烯的化学性质;乙醛的化学性质
【答案解析】Ⅰ. (1) ③④[来源:Zxxk.Com]
(2)2CH3OH+O2催化剂△2HCHO+2H2O
(3)发生氧化反应,若是加成反应,则只生成一种有机物,有机物属于非电解质,不能电离成酸性溶液
Ⅱ.(4)CH3CH2OH浓硫酸170 ℃CH2===CH2↑+H2O
(5)①除去乙烯中的酸性气体,②使乙烯与氢气混合,③观察气泡并调节乙烯与氢气混合的体积之比(只要答出其中两点即可)
(6)CH2===CH2+Br2―→CH2BrCH2Br
(7)②中酸性KMnO4溶液不褪色,点燃气体后附有澄清石灰水的烧杯壁出现白色沉淀
解析:(1)根据实验目的是用甲醇催化氧化法得到甲醛,并且验证甲醛性质,需要与氧气加热反应,所以选装置③④;
(2)甲醇的催化氧化方程式为:2CH3OH+O2催化剂△2HCHO+2H2O;
(3)若是加成反应,则只生成一种有机物,有机物属于非电解质,不能电离成酸性溶液,因此发生的是氧化反应;
(4)实验室制取乙烯的方程式为:CH3CH2OH浓硫酸170 ℃CH2===CH2↑+H2O;[来源:学科网ZXXK]
(5)通过氢氧化钠溶液,可以除去乙烯中的酸性气体、使乙烯与氢气混合、还可以通过观察气泡并调节乙烯与氢气混合的体积之比,故答案为:除去乙烯中的酸性气体、使乙烯与氢气混合,③观察气泡并调节乙烯与氢气混合的体积之比(只要答出其中两点即可);
(6)乙烯易和溴加成生成1,2-二溴乙烷,CH2===CH2+Br2―→CH2BrCH2Br;
(7)若反应后的气体不能够使高锰酸钾溶液褪色,且点燃后生成了二氧化碳,证明了乙烯与氢气反应生成了乙烷,故答案为:②中酸性KMnO4溶液不褪色,点燃气体后附有澄清石灰水的烧杯壁出现白色沉淀;
【思路点拨】本题考查了甲醇催化氧化制取甲醛及乙烯的制取与性质,涉及的内容较多,充分考查了学生分析理解能力及对书写知识的掌握情况,本题难度中等。


科目:高中化学 来源: 题型:
下图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )

A.原子半径:Z>Y>X
B.气态氢化物的稳定性:W>R
C.WX3和水反应形成的化合物是离子化合物[来*源#^@:中国教育出版~网]
D.Y和Z两者最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
为了确认CH3COOH、H2CO3和H2SiO3的酸性强弱,有人设计用下图所示装置,一次实验达到目的(不能再选用其他酸性溶液)。
 |
(1)锥形瓶内盛放上面三种酸中的某种可溶性正盐固体,此固体为 ,分液漏斗中所盛试剂是 ;
(2)装置B中所盛试剂为碳酸氢钠;该试剂的作用是 ;
(3)装置C中出现的现象是 。
(4)现有丙酸(CH3CH2COOH)和醋酸(CH3COOH)关系 (填字母)
甲酸甲酯(HCOOCH3)和醋酸(CH3COOH)关系 (填字母)
A. 同位素B.同分异构C.同系物D.同素异形体E.同一物质
(5)请写出CH3COOH和CH3OH的酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
除去下列物质中所含杂质(括号中的物质)所选用的试剂和装置均正确的是 ( )
Ⅰ.试剂:①KMnO4/H+②NaOH溶液 ③饱和Na2CO3溶液④H2O ⑤Na
⑥Br2/H2O ⑦Br2/CCl4
Ⅱ.装置:

| 选项 | 物质 | 试剂 | 装置 |
| A | C2H6(C2H4) | ⑥ | ① |
| B | 苯(苯酚) | ① | ③ |
| C | CH3COOC2H5(CH3COOH) | ③ | ② |
| D | 甲苯(二甲苯) | ① | ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
天然维生素P(结构如下图,分子结构中R为饱和烃基)存在于槐树花蕾中,它是一种营养增补剂,关于维生素P的叙述正确的是 ( )
 A.可与溴水反应,且1 mol该物质与足量溴水反
A.可与溴水反应,且1 mol该物质与足量溴水反
应消耗6 mol Br2
B.可与NaOH溶液反应,1 mol该物质可与5 mol
NaOH反应
C.一定条件下1 mol该物质可与H2加成,耗H2
最大量为6 mol
D.维生素P能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:
CH3CH2OH-4e—+H2O==CH3COOH+4H+。下列有关说法正确的是
A.检测时,电解质溶液中的H+向负极移动
B.若有 0.4 mol电子转移,则在标准状况下消耗 4.48 L氧气
C.电池反应的化学方程式为:CH3CH2OH+O2===CH3COOH+H2O
D.正极上发生的反应为:O2+4e-+2H2O===4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
无水AlCl3可用作有机合成的催化剂、食品膨松剂等。工业上由铝土矿(主要成分是A12O3和Fe2O3)和石油焦(主要成分是C)按下图所示流程进行一系列反应来制备无水AlCl3。
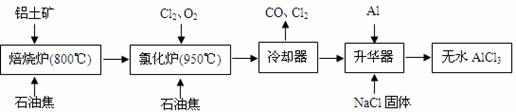
(1)氯化铝在加热条件下易升华,气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则AlCl3是 晶体,其结构式为 。
(2)氯化炉中Al2O3、Cl2和C反应的化学方程式是 。
(3)冷却器排出的尾气中含有大量CO和少量Cl2,需用Na2SO3溶液除去Cl2,此反应的离子方程式为: 。
(4)升华器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是: 。
(5)AlCl3产品中Fe元素含量直接影响其品质,为测定产品中Fe元素的含量,现称取16.25g无水AlCl3产品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重残留固体质量为0.32g。则产品中Fe元素的含量为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
草木灰中含有可溶性钾盐(主要成分是K2SO4、K2CO3、KCl)。某学生按下列操作提取草木灰中的钾盐:①取草木灰加水溶解;②过滤.取滤液;③蒸发滤液;④冷却结晶。为检验草木灰中的阴离子,取少量晶体溶于水,并把溶液分成三等分:
①取一份溶液,加入适量HCl,观察到____________________________,证明含有碳酸根。
②取另一份溶液,为检验SO42-,应往溶液中先加入过量的_______,再加入BaCl2溶液。
③取剩余的一份溶液,加适量的硝酸银,观察到有沉淀产生,该生由此证明溶液中一定含Cl-。你认为所得的结论是否严密?______。理由是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com