
【题目】按要求书写下列化学方程式:
(1)丙烯的加聚
(2)1,3﹣丁二烯与等物质的量的单质溴在60℃时发生1,4﹣加成
(3)甲苯制备TNT
(4)1,2﹣二溴乙烷与氢氧化钠水溶液共热:
(5)乙醛的还原:
(6)乙二醇和乙二酸脱水成二元环酯 .
【答案】
(1)![]()
(2)CH2=CH﹣CH=CH2+Br2→CH2Br﹣CH=CH﹣CH2Br
(3)
(4)CH2BrCH2Br+2NaOH ![]() CH2OHCH2OH+2NaBr
CH2OHCH2OH+2NaBr
(5)CH3CHO+H2 ![]() CH3CH2OH
CH3CH2OH
(6)HOCH2CH2OH+HOOCCOOH ![]()
 +2H2O
+2H2O
【解析】解:(1)丙烯发生加聚反应生成聚丙烯,化学方程式为: ![]() ;
;
所以答案是: ![]() ;(2)60℃时1,3﹣丁二烯与溴1:1发生1,4加成反应生成1,4﹣二溴﹣2﹣丁烯,反应方程式为CH2=CH﹣CH=CH2+Br2→CH2Br﹣CH=CH﹣CH2Br,
;(2)60℃时1,3﹣丁二烯与溴1:1发生1,4加成反应生成1,4﹣二溴﹣2﹣丁烯,反应方程式为CH2=CH﹣CH=CH2+Br2→CH2Br﹣CH=CH﹣CH2Br,
所以答案是:CH2=CH﹣CH=CH2+Br2→CH2Br﹣CH=CH﹣CH2Br;(3)甲苯与浓硝酸、浓硫酸发生取代反应生成TNT,反应为  ,
,
所以答案是:  ;(4)卤代烃在碱性水溶液加热条件下发生取代反应,由1,2﹣二溴乙烷变成乙二醇,方程式为CH2BrCH2Br+2NaOH
;(4)卤代烃在碱性水溶液加热条件下发生取代反应,由1,2﹣二溴乙烷变成乙二醇,方程式为CH2BrCH2Br+2NaOH ![]() CH2OHCH2OH+2NaBr,
CH2OHCH2OH+2NaBr,
所以答案是:CH2BrCH2Br+2NaOH ![]() CH2OHCH2OH+2NaBr;(5)乙醛与氢气在催化剂条件下发生加成反应生成乙醇,方程式:CH3CHO+H2
CH2OHCH2OH+2NaBr;(5)乙醛与氢气在催化剂条件下发生加成反应生成乙醇,方程式:CH3CHO+H2 ![]() CH3CH2OH;
CH3CH2OH;
所以答案是:CH3CHO+H2 ![]() CH3CH2OH;(6)乙二酸和乙二醇之间可以发生酯化反应得到乙二酸乙二醇酯,方程式:HOCH2CH2OH+HOOCCOOH
CH3CH2OH;(6)乙二酸和乙二醇之间可以发生酯化反应得到乙二酸乙二醇酯,方程式:HOCH2CH2OH+HOOCCOOH ![]()
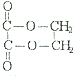 +2H2O;
+2H2O;
所以答案是:HOCH2CH2OH+HOOCCOOH ![]()
 +2H2O;
+2H2O;


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】将一定质量的镁铝合金投入100mL稀硝酸中完全溶解,反应过程中无气体放出。向反应后的溶液中,逐滴加入1.00 mol/L NaOH溶液,加入NaOH溶液的体积与产生沉淀的物质的量关系如图所示,则下列说法错误的是

A. 合金中镁铝的物质的量之比为1:2
B. 合金完全溶解转移电子的物质的量为0. 032mol
C. 原稀硝酸的物质的量浓度为0. 45 mol/L
D. F点溶液中,溶质仅为Na[Al(OH)4]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在相应的条件下一定能大量共存的是( )
A.在碱性溶液中:CO32﹣、K+、S2﹣、Na+
B.与铝粉反应放出氢气的无色溶液中:NO3﹣、Mg2+、Na+、SO42﹣
C.在 ![]() ?=1×1012的溶液中:NH4+、AlO2﹣、C1﹣、K+
?=1×1012的溶液中:NH4+、AlO2﹣、C1﹣、K+
D.在中性溶液中:Fe3+、C1﹣、NO3﹣、A13+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验,能成功的是( )
A.苯和溴水、铁屑混合制溴苯
B.用溴水除乙烷中混有的乙烯
C.苯与浓硝酸和浓硫酸的混合物共热至70℃~80℃制硝基苯
D.用酒精和浓盐酸通过加热来制取乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次增大的短周期元素a、b、c、d和e中,a的最外层电子数为其周期数的二倍;b和d的A2B型氢化物均为V形分子,c的+1价离子比e的﹣1价离子少8个电子. 回答下列问题:
(1)元素c为;d为
(2)由这些元素形成的双原子分子为 .
(3)这些元素的单质或由它们形成的AB型化合物中,其晶体类型属于原子晶体的是 , 离子晶体的是 , 金属晶体的是 , 分子晶体的是;(每空填一种)
(4)元素a和b形成的一种化合物与c和b形成的一种化合物发生的反应常用于防毒面具中,两种化合物的电子式分别为:、 , 该反应的化学方程式为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。
已知:①Se+2H2SO4(浓)===2SO2↑+SeO2+2H2O; ②2SO2+SeO2+2H2O===Se+2 SO42-+4H+。
(1)Se与浓H2SO4的反应中,氧化剂是__________,还原剂是___________,反应中被还原的元素是________。当有标准状况下22.4 L SO2气体生成时,转移电子的物质的量是________ mol。
(2)依据反应①、②判断SeO2、浓H2SO4、SO2的氧化性由强到弱的顺序是______________________________________________________________________。
(3)用双线桥法标出反应②电子转移的方向和数目:_____________________________________。
(4)SeO2、KI和HNO3发生如下反应:SeO2+KI+HNO3→Se+I2+KNO3+H2O
配平上述反应的化学方程式。________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室用固体烧碱配制500mL 0.10 mol·L-1的NaOH 溶液,需要称取______g固体,称量NaOH固体时需要的仪器有_____________________,定容时所需的仪器有________________。
(2)实验室要用98%(ρ=1.84g·cm-3)的硫酸配制0.5mol·L-1的硫酸溶液250mL,需准确量取98%的硫酸_______mL,需要选择_______ml量筒。
(3)若配制0.5mol·L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,下列所配制的硫酸溶液浓度偏低的是_________________________。
A.将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒。
B.移液时容量瓶中有少量蒸馏水
C.用胶头滴管向容量瓶中加水时溶液凹面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切。
D.用胶头滴管加水时,俯视观察溶液凹液面与容量瓶刻度相切。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列叙述错误的是
A. 干电池工作时将化学能转化为电能B. 医用酒精是纯酒精
C. 食盐溶解于水时破坏了化学键D. 人工固氮是氮的循环的一部分
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com