
分析 (1)根据配制步骤是计算、称量、溶解、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;
(2)根据n=cV和m=nM来计算;
(3)容量瓶是精确仪器,仪器上标有温度、刻度线和容量;
(4)根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析.
解答 解:(1)操作步骤有计算、称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以所需的玻璃仪器有烧杯、玻璃棒、100mL容量瓶、胶头滴管,
故答案为:玻璃棒;100mL容量瓶;
(2)配制1.00mol/L的NaCl溶液0.1L所需的氯化钠的物质的量n=cV=1mol/L×0.1L=0.1mol/L,质量m=nM=0.1mol×58.5g/mol=5.85g,托盘天平精确到0.1g,本实验需称量氯化钠(NaCl)质量为5.9g,
故答案为:5.9;
(3)因容量瓶是配制一定浓度、一定体积溶液的精确仪器,受温度、体积的影响,上标有温度、容量、刻度线,
故答案为:温度;容量;
(4)①若定容时俯视读数,未加水到刻度线,溶液体积小,会导致所配溶液浓度偏高,故答案为:偏高;
②配制溶液最后需要加水定容,若用未经干燥的容量瓶去配制溶液,对配制溶液浓度无影响,故答案为:无影响.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度和减小压强 | B. | 降低温度和减小压强 | ||
| C. | 降低温度和增大压强 | D. | 升高温度和增大压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ),三聚磷酸钠是常用的水处理剂,次磷酸钠(Nail2Pa)可用于化学镀镍等等.完成下列填空:
),三聚磷酸钠是常用的水处理剂,次磷酸钠(Nail2Pa)可用于化学镀镍等等.完成下列填空:
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
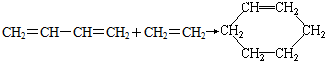
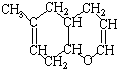 两种有机物的结构简式
两种有机物的结构简式 ;
;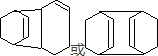 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四种元素位于同一周期 | B. | 氢化物的稳定性H2Y>HZ | ||
| C. | 离子的氧化性aW3+>bX+ | D. | 原子序数:c>b |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

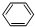 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$ +HBr;
+HBr;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com