
在25℃时,将两个铜电极插入一定量的硫酸钠饱和溶液中进行电解,通电一段时间后,
阴极逸出a mol气体,同时有w g Na2SO4·10H2O晶体析出,若温度不变,剩余溶液中
溶质质量分数是( )。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
在0.lmol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH  CH3COO-+H+ 对于该平衡,下列叙述正确的是
CH3COO-+H+ 对于该平衡,下列叙述正确的是
A.加入少量CH3COONa固体,平衡向逆向移动,溶液导电能力增强
B.加入少量NaOH固体,平衡向正向移动,溶液中c(H+)增大
C.加水,平衡向正向移动, c(CH3COOH)/ c(CH3COO-)增大
D.通入少量 HCl气体,平衡逆向移动,溶液中c(H+)减少
查看答案和解析>>
科目:高中化学 来源: 题型:
A和B均为短周期元素,它们的离子A-和B2+具有相同的核外电子层结构。下面说法正确的是
A.原子序数A > B B.核外电子数A > B
C. 原子半径A > B D.离子半径 A- > B2+
查看答案和解析>>
科目:高中化学 来源: 题型:
各类化合物与单质处于固态(晶体)时,构成晶体的粒子间必定存在一定形式的相互作用,粒子按一定规律在空间整齐排列,形成几何晶体。
(1)当构成晶体的粒子为阴、阳离子时,这种晶体称为 ,微粒间的作用是 ,由于这种作用较 ,一般说来,这种晶体有 的熔、沸点和 的硬度。
(2)当构成晶体的粒子为分子时,这种晶体称为 ,微粒间的作用是 ,由于这种作用 ,一般说来,这种晶体有较低的熔、沸点和 的硬度。
(3)当构成晶体的粒子为原子时,这种晶体称为 ,由于这种晶体的微粒之间全部以 结合,并形成一种 结构,故这种晶体具有 的熔、沸点 和 的硬度。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液肯定呈酸性的是( )
A.含有H+离子的溶液 B. c(OH-)=1×10-8mol/L的溶液
C. c(OH-)<c(H+)的溶液 D. pH小于7的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列烷烃沸点由高到低顺序正确的是( )
①丁烷 ②2-甲基丙烷 ③戊烷 ④2-甲基丁烷 ⑤2,2-二甲基丙烷
A. ①②③④⑤ B. ⑤④③②①
C. ②①⑤④③ D. ③④⑤①②
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙两池的电极材料如图所示,请按要求回答下列问题:
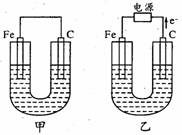
(1)若两池中均为Cu(NO3)2溶液,反应一段时间后:
①有红色物质析出的是甲池中的 (填“铁”或“碳”)棒;乙池中的 (填“阴”或“阳”)极。
②乙池中阳极上发生的电极反应方程式是 。
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的化学方程式: 。
②甲池中碳极上电极反应方程式是 ,乙池碳极上
电极反应属于 (填“氧化反应”或“还原反应”)。
③将湿润的淀粉KI试纸放在乙池碳极附近,发现试纸变蓝,待一段时间后又发现
蓝色褪去。这是因为过量的Cl2将生成的I2又氧化。若反应的C12和I2物质的量
之比为5:1,且生成HCl和另一种强酸,该强酸的化学式为 。
④若乙池中转移0.1 mol e-后停止实验,池中溶液体积是1L,则溶液混匀后的pH= (不考虑所生成的气体溶解在溶液中的情况)
查看答案和解析>>
科目:高中化学 来源: 题型:
要检验溴乙烷中的卤素是不是溴元素,正确的实验方法是 ( )
①加入氯水振荡,观察水是否有红棕色的溴出现
②加入NaOH溶液共热,冷却后加入稀硝酸至酸性,再滴入AgNO3溶液,观察有无浅黄
色沉淀生成
③滴入AgNO3溶液,再加入稀硝酸,观察有无浅黄色沉淀生成
④加入NaOH的醇溶液共热,冷却后加入稀硝酸至酸性,再滴入AgNO3溶液,观察有无
浅黄色沉淀生成
A.①③ B.②④ C.①② D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各表述与示意图一致的是

A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应2SO2 (g) + O2(g)  2SO3(g) ΔH < 0 ,正、逆反应的平衡常数K随温度的变化
2SO3(g) ΔH < 0 ,正、逆反应的平衡常数K随温度的变化
C.图③表示10 mL 0.01 mol·L-1 KMnO4 酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化
D.图④中a、b曲线分别表示反应CH2=CH2 (g) + H2(g)→CH3CH3(g) ΔH<0使用(a)和未使用(b)催化剂时,反应过程中的能量变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com