
 .
. HSO3-+OH-(用离子方程式表示).
HSO3-+OH-(用离子方程式表示). 分析 A、B同主族,且能形成BA3型化合物,则A为O、B为S,根据B、C、D的离子电子层结构相同,可知都为18e-微粒,离子半径按照B、C、D的顺序减小,说明B、C、D三元素的原子序数关系为S<C<D,因为D的原子序数小于20,则C为Cl、D为K.
解答 解:A、B同主族,且能形成BA3型化合物,则A为O、B为S,根据B、C、D的离子电子层结构相同,可知都为18e-微粒,离子半径按照B、C、D的顺序减小,说明B、C、D三元素的原子序数关系为S<C<D,因为D的原子序数小于20,则C为Cl、D为K.
(1)K在元素周期表中的位置为第四周期第ⅠA族,
故答案为:第四周期第ⅠA族;
(2)S与K形成化合物的电子式为 ,
,
故答案为: ;
;
(3)将氯水滴加到K2S溶液中发生反应:K2S+Cl2═2KCl+S↓,
故答案为:K2S+Cl2═2KCl+S↓;
(4)除去SO2气体可以用酸性高锰酸钾溶液或NaOH溶液,但是不能用浓硫酸吸收,SO2不溶于浓硫酸,品红只是用来检验SO2的存在,一般不用来除去SO2,
故选:AC;
(5)K2SO3溶液显碱性的原因是SO32-的水解:SO32-+H2O HSO3-+OH-,破坏水的电离平衡,溶液呈碱性,
HSO3-+OH-,破坏水的电离平衡,溶液呈碱性,
故答案为:SO32-+H2O HSO3-+OH-.
HSO3-+OH-.
点评 本题考查结构性质位置关系应用,难度不大,推断元素是解题关键,侧重对化学用语与元素化合物性质的考查,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:推断题
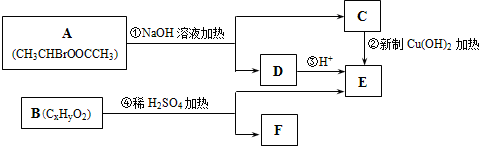
 .
. 、
、 、
、 、
、 任意1种.
任意1种.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
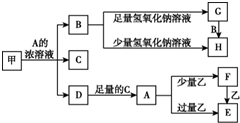 中学化学中常见的几种物质存在如下关系,其中甲是黑色非金属单质,乙是生活中常见的金属单质,D是红棕色气体(图中部分产物和反应条件已略去).
中学化学中常见的几种物质存在如下关系,其中甲是黑色非金属单质,乙是生活中常见的金属单质,D是红棕色气体(图中部分产物和反应条件已略去).查看答案和解析>>
科目:高中化学 来源: 题型:推断题
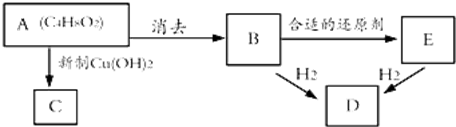
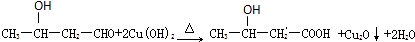 .
.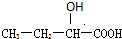 、
、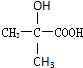 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
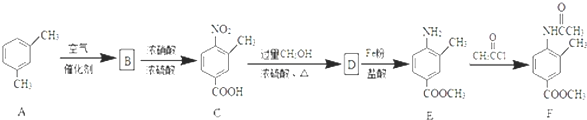
 ;由D→E的反应类型是还原反应.
;由D→E的反应类型是还原反应. .
. .
.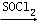 RCOCl.请写出以CH3CH2OH、
RCOCl.请写出以CH3CH2OH、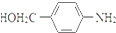 为原料,制备化合物
为原料,制备化合物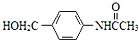 的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:H2C═CH2
的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:H2C═CH2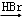 CH3CH2Br
CH3CH2Br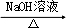 CH3CH2OH.
CH3CH2OH.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
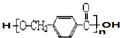 其合成路线如下:
其合成路线如下: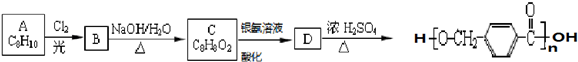
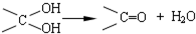
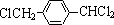 ,其中的官能团名称为氯原子.
,其中的官能团名称为氯原子.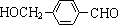 +2Ag(NH3)2OH $\stackrel{△}{→}$
+2Ag(NH3)2OH $\stackrel{△}{→}$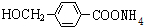 +2Ag↓+3NH3+H2O.由D生成高分子化合物的反应n
+2Ag↓+3NH3+H2O.由D生成高分子化合物的反应n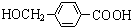 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$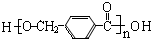 +(n-1)H2O.
+(n-1)H2O.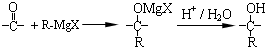
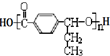 ,在合成过程中所用的格氏试剂的化学式为CH3CH2MgX(用X表示卤原子),合成过程中涉及到的有机化学反应类型有ACD(填编号)
,在合成过程中所用的格氏试剂的化学式为CH3CH2MgX(用X表示卤原子),合成过程中涉及到的有机化学反应类型有ACD(填编号)查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
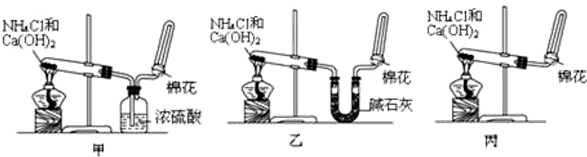
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com