
下列离子方程式书写正确的是( )
A.少量CO2通入Ba(OH)2溶液中:CO2+2OH—= CO32— +H2O
B.NH4Al(SO4)2溶液中滴入Ba(OH)2溶液至SO42—恰好沉淀完全
NH4++Al3++2SO42—+2Ba2++4OH—= NH3·H2O+Al(OH)3↓+2BaSO4↓
C.FeCl3溶液腐蚀铜线路板:Fe3++Cu = Fe2++Cu2+
D.向NaHCO3溶液中滴入少量Ca(OH)2溶液:HCO3—+OH—= CO32—+H2O
科目:高中化学 来源:2014-2015江西省景德镇市高二上学期期中化学(文)试卷(解析版) 题型:简答题
三国时期,诸葛亮领兵南征,遇到了“哑泉”,士兵饮后腹痛,致哑,甚至死亡。又有一“安乐泉”,饮后可解“哑泉”之毒。经科研人员研究,“哑泉”水溶液中有硫酸铜,“安乐泉”水质偏碱性。
(1)请你说出“哑泉”使人中毒的原因。(4分)
(2)“安乐泉”能够解毒的原因是什么?(6分)
(3)现代生活中如果遇到类似“哑泉”中毒的现象,你能用什么办法尽快解毒?(4分)
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高二上学期期中化学(必修)试卷(解析版) 题型:选择题
对于某些离子的检验及结论一定正确的是
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32?
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42?
C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省越秀区高一下学期学业水平测试调研化学试卷(解析版) 题型:选择题
短周期元素甲,乙,丙,丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁原子最外层电子数和电子层数相等,则 ( )
A.原子半径 丁 >丙>乙
B.单质的还原性丁>丙>甲
C.甲,乙,丙的氧化物均为共价化和物
D.乙,丙,丁的最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省越秀区高一下学期学业水平测试调研化学试卷(解析版) 题型:选择题
卤素间形成的化合物如“IF5、BrCl、IBr”等称为卤素互化物,化学性质与卤素单质类似,则下列关于卤素互化物的性质的描述及发生的相关反应不正确的是( )
A.IF5 + 3H2O = HIO3 +5HF
B.3IBr +2Fe = FeI3 + FeBr3
C.BrCl的氧化性强于I2
D.IBr可以与NaOH溶液反应生成2种盐
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省越秀区高一下学期学业水平测试调研化学试卷(解析版) 题型:选择题
下列物质中不能使酸性KMnO4溶液褪色的是( )
①乙烯 ②苯 ③乙醇 ④甲烷 ⑤乙酸 ⑥二氧化硫
A.①②③④⑤ B.②④⑤ C.②④⑤⑥ D.①③⑥
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省肇庆市第二学期高二期末统测化学试卷(解析版) 题型:填空题
电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。 请回答以下问题:
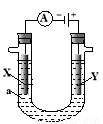
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①在X极附近观察到的现象是 。
②Y电极上的电极反应式是 ;把湿润的碘
化钾淀粉试纸放在Y电极附近,现象是 。
(2)要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:X电极的材料是 ,
Y电极上发生的电极反应式为 。(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省高一下学期期末考试化学试卷(解析版) 题型:填空题
利用“化学蒸气转移法”制备TaS2晶体,某温度下的2L恒容密闭容器中加入一定量 的 I2(g)和TaS2(s)发生如下反应
TaS2(s)+2I2(g) TaI4(g)+S2(g)△H=a kJ·mol-1 (I)
TaI4(g)+S2(g)△H=a kJ·mol-1 (I)
达平衡时,TaS2(s)、I2(g)、TaI4(g)、、S2(g)的物质的量分别为3 mol 、2mol、2mol、2mol。
(1)反应(I)的平衡常数表达式K=
(2)若该温度下该容器中某时刻TaS2(s)、I2(g)、TaI4(g)、、S2(g)的物质的量分别为2mol、2mol、4mol、4mol,则该时刻平衡向 (填“正反应”或“逆反应”)移动,v正 v逆(填“>”、“=”或“<”)。
(3)在不同温度下,该反应的平衡常数K如下表:
温度/℃ | 40 | 80 | 200 |
平衡常数K | 1 | 1.5 | 4 |
该反应的△H 0(填“>”、“=”或“<”)。
(4)40℃时,向该恒容密闭容器中加入2mol I2(g)和4mol TaS2(s),I2(g)的平衡转化率为 (写出计算过程,结果保留小数点后1位)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com