
| A. | 常温下,水电离出的c(H+)=1×10-12 mol/L的溶液中不可能大量存在:Al3+、NH4+、Cl-、S2- | |
| B. | 加入铝粉能产生H2的溶液中可能大量存在:Na+、Cl-、S2-、SO32- | |
| C. | 过量铁粉与稀HNO3反应:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| D. | 向AlCl3溶液中滴入大量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
分析 A.水电离出的c(H+)=1×10-12 mol/L的溶液,水的电离受到抑制,该溶液可能为碱性溶液,也可能为酸性溶液;
B.铝与强碱溶液,酸溶液反应都能生成氢气;
C.铁过量反应生成硝酸亚铁与一氧化氮和水;
D.不符合反应客观事实.
解答 解:A.水电离出的c(H+)=1×10-12 mol/L的溶液,水的电离受到抑制,该溶液可能为碱性溶液,也可能为酸性溶液,酸性溶液中硫离子不共存,碱性溶液中铝离子、铵根离子不共存,故A正确;
B.加入铝粉能产生H2的溶液若为强碱溶液,OH-、Na+、Cl-、S2-、SO32-,相互不反应可以共存,故B正确;
C.过量铁粉与稀HNO3反应,离子方程式:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O,故C正确;
D.向AlCl3溶液中滴入大量氨水反应生成氢氧化铝沉淀和氯化铵:Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故D错误;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质及离子反应条件是解题关键,题目难度不大.


 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:选择题
| A. | 发生水合过程,并且放出热量 | |
| B. | 发生扩散过程,并且放出热量 | |
| C. | 水合过程放出的热量大于扩散过程吸收的热量 | |
| D. | 扩散过程放出的热量大于水合过程吸收的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH (g)和 1mol H2O(g) |
| 平衡时c(CH3OH) | c1 | c2 |
| 平衡时能量变化 | 放出29.4kJ | 吸收a kJ |
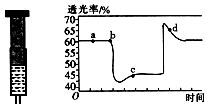
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对盛在烧杯(敞口)内的氨水加热,氨水中NH4+浓度减小 | |
| B. | 对2HI(g)?H2(g)+I2(g),保持容器体积不变,通入氢气可使平衡体系颜色变浅 | |
| C. | 500℃左右比室温更有利于合成氨的反应 | |
| D. | 高压有利于合成氨的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④>②>③>① | B. | ①>④>②>③ | C. | ①>②>③>④ | D. | ④>①>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
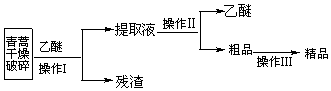
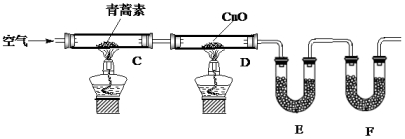
| 装置 | 实验前 | 实验后 |
| E | 24.00g | 33.90g |
| F | 100.00g | 133.00g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
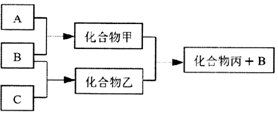 如图所示转化关系中A、B、C均为双原子气态单质,分别由短周期主族元素X、Y、Z组成.其中单质B含共用电子对数最多,甲和丙分子中均含有10个电子.下列说法错误的是( )
如图所示转化关系中A、B、C均为双原子气态单质,分别由短周期主族元素X、Y、Z组成.其中单质B含共用电子对数最多,甲和丙分子中均含有10个电子.下列说法错误的是( )| A. | Z元素位于第二周期第VIA族 | |
| B. | 可用排水法收集化合物乙 | |
| C. | 元素X、Y、Z的原子半径大小关系为X<Z<Y | |
| D. | 化合物甲溶于化合物丙中,存在的微粒有5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去Cl2的HCl气体可以通过浓硫酸 | |
| B. | 碳酸钠固体中的碳酸氢钠杂质可以通过加热除去 | |
| C. | SO2可以通过碱石灰干燥 | |
| D. | FeCl3溶液中含有CuCl2可以加入足量NaOH溶液除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com