
 Ģ¼ŗĶĢ¼µÄ»ÆŗĻĪļŌŚÉś²ś”¢Éś»īÖŠµÄÓ¦ÓĆ·Ē³£¹ć·ŗ£¬ŌŚĢį³«½”æµÉś»īŅŃ³É³±Į÷µÄ½ńĢģ£¬”°µĶĢ¼Éś»ī”±²»ŌŁÖ»ŹĒŅ»ÖÖĄķĻė£¬øüŹĒŅ»ÖÖÖµµĆĘŚ“żµÄŠĀµÄÉś»ī·½Ź½£®
Ģ¼ŗĶĢ¼µÄ»ÆŗĻĪļŌŚÉś²ś”¢Éś»īÖŠµÄÓ¦ÓĆ·Ē³£¹ć·ŗ£¬ŌŚĢį³«½”æµÉś»īŅŃ³É³±Į÷µÄ½ńĢģ£¬”°µĶĢ¼Éś»ī”±²»ŌŁÖ»ŹĒŅ»ÖÖĄķĻė£¬øüŹĒŅ»ÖÖÖµµĆĘŚ“żµÄŠĀµÄÉś»ī·½Ź½£®·ÖĪö £Ø1£©¢Ł2CH4£Øg£©+3O2£Øg£©=2CO£Øg£©+4H2O£Øl£©”÷H=-1214kJ/mol
¢Ś2CO£Øg£©+O2£Øg£©=2CO2£Øg£©”÷H=-566kJ/mol
ÓÉøĒĖ¹¶ØĀÉæÉÖŖ£¬$\frac{¢Ł+¢Ś}{2}$$\frac{¢Ł-¢Ś}{2}$µĆµ½CH4£Øg£©+2O2£Øg£©=CO2£Øg£©+2H2O£Øl£©£»
£Ø2£©øŗ¼«ÉĻ¼×Ķ鏧Ȅµē×ÓÉś³ÉĢ¼ĖįøłĄė×Ó£»
£Ø3£©A£®A¶Ė×öŃō¼«ŹĒĢś£¬B¶ĖĪö³öĒāĘųæÉĒżøĻŌČÜŅŗÖŠČܽāµÄÉŁĮæŃõĘų£»
B£®Ńō¼«ÉĻĢśŹ§µē×ӵƵ½ŃĒĢśĄė×Ó£¬Ņõ¼«ÉĻĒāĄė×ӷŵē£¬ĖłŅŌæÉŅŌµē½āÖŹČÜŅŗæÉŅŌєȔĀČ»ÆÄĘČÜŅŗ£»
C£®Ńō¼«Ó¦øĆÓĆĢśµē¼«£¬Ņõ¼«ÓƶčŠŌµē¼«ŅąæÉ£»
D£®Ņõ¼«ÉĻµĆµē×ÓÉś³ÉĒāĘų£®
½ā“š ½ā£ŗ£Ø1£©¢Ł2CH4£Øg£©+3O2£Øg£©=2CO£Øg£©+4H2O£Øl£©”÷H=-1214kJ/mol
¢Ś2CO£Øg£©+O2£Øg£©=2CO2£Øg£©”÷H=-566kJ/mol
ÓÉøĒĖ¹¶ØĀÉæÉÖŖ£¬$\frac{¢Ł+¢Ś}{2}$$\frac{¢Ł-¢Ś}{2}$µĆµ½CH4£Øg£©+2O2£Øg£©=CO2£Øg£©+2H2O£Øl£©£¬”÷H=$\frac{-1214+£Ø-566£©}{2}$kJ/mol=-890kJ/mol£¬
¼×ĶéČ¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½ĪŖCH4£Øg£©+2O2£Øg£©=CO2£Øg£©+2H2O£Øl£©”÷H=-890kJ/mol£¬
¹Ź“š°øĪŖ£ŗCH4£Øg£©+2O2£Øg£©=CO2£Øg£©+2H2O£Øl£©”÷H=-890kJ/mol£»
£Ø2£©¼īŠŌ¼×ĶéČ¼ĮĻµē³Ų£¬¾ßÓŠ»¹ŌŠŌµÄČ¼ĮĻ¼×ĶéĪŖŌµē³ŲµÄøŗ¼«£¬·¢ÉśŃõ»Æ·“Ó¦£¬µē¼«·“Ó¦Ź½ĪŖCH4+10OH--8e-=CO32-+7H2O£¬
¹Ź“š°øĪŖ£ŗCH4+10OH--8e-=CO32-+7H2O£»
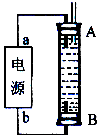
£Ø3£©A£®ŅņĪŖÉś³ÉµÄĒāĘų½«×°ÖĆÖŠŌÓŠŃõĘų“ų³ö£¬ĒŅĒāĘųµÄĆܶȊ”ÓŚĖ®£¬ĖłŅŌĒāĘų“ÓB¶ĖŅõ¼«Īö³ö£¬Aµē¼«ŌņŹĒĢś×öŃō¼«Ź§Č„µē×ÓÉś³ÉŃĒĢśĄė×Ó£¬ĖłŅŌ”°a”±ĪŖÕż¼«£¬”°b”±ĪŖøŗ¼«£¬¹ŹAÕżČ·£»
B£®ŅņĪŖŃō¼«ŹĒĢś£¬»īĘƵē¼«×÷Ńō¼«Ź±£¬Ńō¼«²ÄĮĻĢśŹ§µē×ÓÉś³ÉŃĒĢśĄė×Ó£¬Ņõ¼«ÉĻĒāĄė×ӷŵē£¬Éś³ÉĒāĘų£¬ĖłŅŌÄÜÉś³ÉĒāŃõ»ÆŃĒĢś°×É«³Įµķ£¬Ōņµē½āŅŗŃ”ÓĆNaClČÜŅŗ²»Ó°ĻģŹµŃ飬¹ŹBÕżČ·£»
C£®Ńō¼«Ó¦øĆÓĆĢśµē¼«£¬Ņõ¼«æÉŅŌŹĒĢśŅ²æÉŅŌŹĒĘäĖū¶čŠŌµē¼«£¬¹ŹC“ķĪó£»
D£®Ńō¼«Ó¦øĆÓĆĢśµē¼«£¬Ņõ¼«æÉŅŌŹĒĢśŅ²æÉŅŌŹĒĘäĖū¶čŠŌµē¼«£¬Ņõ¼«ÉĻĖ®µĆµē×ÓÉś³ÉĒāĘųŗĶĒāŃõøłĄė×Ó£¬ĒāĘųÄÜ·ĄÖ¹ĒāŃõ»ÆŃĒĢś±»Ńõ»Æ¶ųµ¼ÖĀŹµŃ鏧°Ü£¬ĖłŅŌµē¼«·“Ó¦Ź½ĪŖ2H++2e-=H2”ü»ņ2H2O+2e-ØTH2”ü+2OH-£¬¹ŹDÕżČ·£»
¹Ź“š°øĪŖ£ŗABD£®
µćĘĄ ±¾Ģāæ¼²éČČ»Æѧ·½³ĢŹ½¼°µē»Æѧ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕøĒĖ¹¶ØĀɵÄÓ¦ÓĆ”¢µē¼«·“Ó¦µÄŹéŠ“ĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬×ŪŗĻŠŌ½ĻĒ棬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū¢Ü | B£® | ¢Ū¢Ł¢Ś¢Ü | C£® | ¢Ü¢Ś¢Ū¢Ł | D£® | ¢Ł¢Ū¢Ś¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
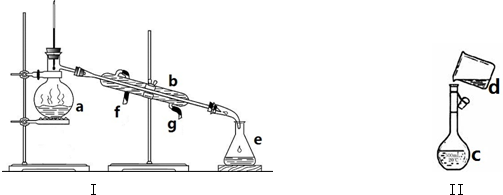
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1£¬3-¶”¶žĻ© | B£® | »·¶”¶žĻ© | C£® | 2-¶”Č² | D£® | 1-¶”Č² |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µ±ĖüĆĒµÄŃ¹ĒæŗĶĢå»ż”¢ĪĀ¶Č¾łĻąĶ¬Ź±£¬ČżÖÖĘųĢåµÄÖŹĮæ£ŗm£ØH2£©£¾m£ØO2£©£¾m£ØCO2£© | |
| B£® | µ±ĖüĆĒµÄĪĀ¶ČŗĶŃ¹Ēæ¾łĻąĶ¬Ź±£¬ČżÖÖĘųĢåµÄĆÜ¶Č£ŗ¦Ń£ØH2£©£¾¦Ń£Ø02£©£¾¦Ń£ØC02£© | |
| C£® | µ±ĖüĆĒµÄÖŹĮæŗĶĪĀ¶Č”¢Ń¹Ēæ¾łĻąĶ¬Ź±£¬ČżÖÖĘųĢåµÄĢå»ż£ŗV£ØCO2£©£¾V£ØO2£©£¾V£ØH2£© | |
| D£® | µ±ĖüĆĒµÄĪĀ¶ČŗĶĆܶȶ¼ĻąĶ¬Ź±£¬ČżÖÖĘųĢåµÄŃ¹Ēæ£ŗP£ØH2£©£¾P£ØO2£©£¾P£ØCO2£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
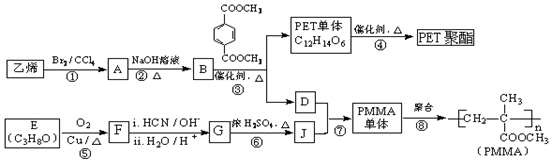
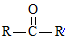 $”ś_{ii£®H_{2}O/H+}^{i£®HCN/OH-}$
$”ś_{ii£®H_{2}O/H+}^{i£®HCN/OH-}$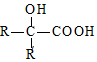 £ØR”¢R”ä“ś±ķĢž»ł£©
£ØR”¢R”ä“ś±ķĢž»ł£© £®
£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū | B£® | ¢Ś¢Ū | C£® | ¢Ū¢Ü | D£® | ¢Ł¢Ś¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| ĪļÖŹ±ąŗÅ | ĖłŹōĄą±š±ąŗÅ | ĪļÖŹ±ąŗÅ | ĖłŹōĄą±š±ąŗÅ |
| £Ø1£© | £Ø4£© | ||
| £Ø2£© | £Ø5£© | ||
| £Ø3£© | £Ø6£© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com