
| 元素代号 | X | Y | Z | W | N |
| 原子半径/nm | 0.186 | 0.074 | 0.102 | 0.099 | 0.160 |
| 主要化合价 | +1 | -2 | -2、+6 | +7、-1 | +2 |
| A、常温下单质与水反应速率:X>N |
| B、最高价氧化物对应水化物酸性:W>Z |
| C、X 与W形成的化合物是共价化合物 |
| D、X和Y的单质在一定条件下反应可生成一种淡黄色的固体化合物 |


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:
A、2CH3CH2OH+O2
| |||
B、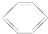 +HNO3 +HNO3
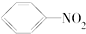 +H2O +H2O | |||
C、CH3CH2OH+CH3COOH
| |||
D、CH4+Cl2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知:2CO(g)+O2(g)=2CO2(g)△H=-566kJ/molNa2O2(s)+CO2(g)=Na2CO3(s)+
已知:2CO(g)+O2(g)=2CO2(g)△H=-566kJ/molNa2O2(s)+CO2(g)=Na2CO3(s)+| 1 |
| 2 |
| A、CO的燃烧热为-283 kJ |
| B、如图可表示由CO生成CO2的反应过程和能量关系 |
| C、2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)△H>-452 kJ/mol |
| D、CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移总数为6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 加热、加压 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2 |
| B、KMnO4 |
| C、FeCl3 |
| D、HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| H2(g) | Br2(g) | HBr(g) | |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 |
| A、200 | B、230 |
| C、260 | D、404 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com