
 �����������һ����Ҫ�Ĺ�ҵԭ�ϣ�ij��ѧС���������ͼװ�ã��Ա����ᡢ�״�Ϊԭ����ȡ������������й����ʵ��������ʼ��±���ʾ��
�����������һ����Ҫ�Ĺ�ҵԭ�ϣ�ij��ѧС���������ͼװ�ã��Ա����ᡢ�״�Ϊԭ����ȡ������������й����ʵ��������ʼ��±���ʾ��
| ������ | �״� | ��������� | |
| �۵�/�� | 122.4 | -97 | -12.3 |
| �е�/�� | 249 | 64.3 | 199.6 |
| �ܶ�/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
| ˮ���� | �� | ���� | ���� |
�ϳɱ���������ֲ�Ʒ
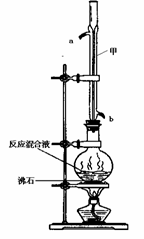
��Բ����ƿ�м���0.1mol�������0.4mol �״�,��С�ļ��� 3mLŨ���ᣬ���Ⱥ�Ͷ�뼸����ʯ��С�ļ���ʹ��Ӧ��ȫ���ñ���������ֲ�Ʒ��
��1����װ�õ������ǣ� ����ȴˮ�� ���a����b�����ڽ��롣
��2����ѧС����ʵ�����ù����ķ�Ӧ��״����������� ��
�ֲ�Ʒ�ľ���
����������ֲ�Ʒ���������������״������ᡢ�������ˮ�ȣ��������������̽��о���

��1���Լ�1������ �����ţ��������� ��
A.ϡ���� B.̼������Һ C. �Ҵ�
��2������2�У��ռ���Ʒʱ�����Ƶ��¶�Ӧ�� �����ҡ�
��3��ʵ���Ƶõı����������Ʒ����Ϊ10g�������ת����Ϊ �����������λ��Ч���֣���
��4����ʵ���Ƶõı���������IJ����������۲��������ܵ�ԭ���� �����ţ���
A������ʱ��100�濪ʼ�ռ���Ʒ B���״��������� C���Ʊ���Ʒʱ�����ᱻ����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
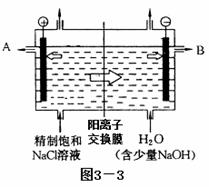
��ҵ�ϵ���Ƽ�ļ������������ӽ���Ĥ������Ҫԭ���DZ���ʳ��ˮ����ͼ3
��3Ϊ�����ӽ���Ĥ�����ԭ��ʾ��ͼ��
 ��ش��������⣺
��ش��������⣺
��1��A��Ϊ���۵�________����B���IJ��Ϲ�ҵ�ϳ����õ��������г����Ľ��������д�����ģ�����Ҫԭ���� �����������ʴ�������ⸯʴ����
��2�������в��������ӽ���Ĥ�ѵ��۸����������Һ������ң����������ӽ���Ĥ��ֻ������Һ�е�__________ͨ������д�������ı�ţ���
��H2����Cl2����H+����Cl-����Na+����OH-��
��3�����������������������ӽ���Ĥ���������ӽ���Ĥ����֪��3Cl2 +6OH-==5Cl-+ClO3-+3H2O��������˵����ȷ������� ��
A��������ʱ���Ҳ���Һ�к���ClO3��
B�������ڷ�����Ӧ���ܻ�ѧ����ʽΪ��NaCl + 3H2O  NaClO3 + 3H2��
NaClO3 + 3H2��
C���������ӽ���Ĥ�����������缫�����ĵ缫��Ӧ��ԭ��һ��
D���������ӽ���Ĥ�������ӵĶ����ƶ�������ԭ���෴
��4����֪ij����ÿСʱ����10%������������Һa kg��ÿСʱ�ܲ�����״���µ�����b L�����������������������Һ���ܶ�Ϊd g��cm-3�������ʵ���Ũ��Ϊ�����ۼ��㣬�軯�� mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£����и���������ָ����Һ��һ���ܴ���������� ��������
A��0.1 mol��L��1 FeCl3��Һ��K����NH4+��I����SCN��
B��0.1 mol��L��1 Na2CO3��Һ��K����Ba2����NO3����Cl��
C��0.1 mol��L��1 NaOH��Һ��K����Na����SO42����CO32��
D��c(H��)/c(OH��)��1��1014����Һ��Ca2����Na����ClO����NO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и������µ��������һ���ܴ���������ǣ� ��
A��c(HCO3��)=1��10��1mol/L����Һ��Na+��AlO2����CH3COO����K+
B����ˮ�������c(H+)=1��10��14mol/L����Һ��CO32����NH4+��SO42����K+
C�����ȳʺ�ɫ����Һ��Fe2+��Cl����NO3����Na+
D����ʹpH��ֽ�ʺ�ɫ����Һ��Mg2+��Cl����NO3����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������Һ���й����ʵ���Ũ�ȹ�ϵ��ȷ���ǣ�������
A��0��1 mol/L pH=3��H2A��Һ��0��01 mol/L pH=11��MOH��Һ����Ȼ�ϣ�
c��H������c��M������c��OH������2c��A2����
B��pH��ȵ�CH3COONa��NaOH��Na2CO3������Һ��
c��NaOH����c��CH3COONa����c��Na2CO3��
C�����ʵ���Ũ�����CH3COOH��CH3COONa��Һ�������ϣ�
c��CH3COO������2c��OH������2c��H������c��CH3COOH��
D��0��1 mol��L��1��NaHA��Һ����pH��4��
c��HA������c��H������c��H2A����c��A2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1���������ƳɵĽ���ȼ�ϡ��ǽ�������ȼ�ϡ���������Ӧ�õ��������߿Ƽ�����λ������A��B����ȼ��ʱ���ų������ȣ�������ȼ�ϡ���֪A��BΪ������Ԫ�أ���ԭ�ӵĵ�һ�����ĵ��������±���ʾ��
| �����ܣ�kJ/mol�� | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1541 | 7733 | 10540 |
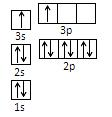
��ijͬѧ����������Ϣ���ƶ�B�ĺ�������Ų�����ͼ��ʾ����ͬѧ�����ĵ����Ų�ͼΥ���� ��BԪ��λ�����ڱ���������е� _______����
 ��ACl2������A���ӻ�����Ϊ ��ACl2�Ŀռ乹��Ϊ ��
��ACl2������A���ӻ�����Ϊ ��ACl2�Ŀռ乹��Ϊ ��
��2��Feԭ�ӻ�������Χ�н϶���������Ŀչ������һЩ���ӻ������γ�����
����Feԭ�ӻ������γ������ķ��ӻ�����Ӧ�߱��Ľṹ������ ��
���������������[Fe(CN)6]4������� ��
A.���ۼ� B.�Ǽ��Լ� C.��λ�� D.�Ҽ� E.�м�
��д��һ���� CN����Ϊ�ȵ�����ĵ��ʷ���ʽ ��
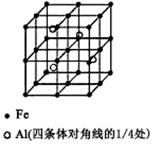
��3��һ��Al��Fe�Ͻ�����徧������ͼ��ʾ����ݴ˻ش��������⣺
��ȷ���úϽ�Ļ�ѧʽ ��
����������ܶȣ��� g/cm3����˺Ͻ������������Feԭ��֮��ľ���(�ú��ѵĴ���ʽ��ʾ�����ػ���)Ϊ cm��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����и������ʵıȽϣ���ȷ���ǣ�������
�����ԣ�HClO4>HBrO4>HIO4 �����ӻ�ԭ�ԣ�S2->Cl->Br ->I- �۷е㣺HF��HCl��HBr>HI
�ܽ����ԣ�K>Na>Mg>Al ����̬�⻯���ȶ��ԣ�HF��HCl��H2S �ް뾶��O2->Na+>Na>Cl
A���٢ڢ� B���ڢۢ� C���٢ܢ� D���٢ڢۢܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ѧ֪ʶ�����ܸ��¿Ƽ�����¶α��ѧ�ǿ�ѧ�����ߵ��������и�������������α��ѧ����( )
A���з���Ч�Ͷ���ũҩ�������߲˵�ũҩ������
B��������ʳƷ���Ӽ���ʳ������彡�����к�������ʳ��
C���붹��ֲ�ﹲ���ĸ��������Խ�����������̬�ĵ�ת��Ϊ�����Ļ�����
D���ڸ��¡���ѹ�ʹ��������£���ʯīת��Ϊ���ʯ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�л����������̼���⡢������Ԫ����ɣ�����Է�������С��150������֪����������������Ϊ50%���������̼ԭ�ӵĸ������Ϊ�� ��
A 4 B 5 C 6 D 7
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com