
 、SO32—、SO42—、Fe2+、Fe3+、K+,按如下流程进行实验:
、SO32—、SO42—、Fe2+、Fe3+、K+,按如下流程进行实验:
| A.现象3不能证明X中是否含有SO42— |
| B.现象2气体C中至少有一种是CO2或SO2,操作Ⅰ为过滤 |
C.现象5表明X溶液中一定含有Cl |
| D.现象1表明X溶液显酸性,沉淀D为Fe(OH)3 |
 ,错误;D、现象1表明X溶液显酸性,沉淀D为Fe(OH)3,正确。
,错误;D、现象1表明X溶液显酸性,沉淀D为Fe(OH)3,正确。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.铁粉中混有铝粉:加入过量烧碱溶液充分反应、过滤 |
| B.CO2中混有HCl:将其通入NaOH溶液 |
| C.NaHCO3溶液中混有少量Na2CO3:往该溶液中通入过量CO2气体 |
| D.NaCl溶液中混有少量I2:加入适量CCl4,振荡,静置,分液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
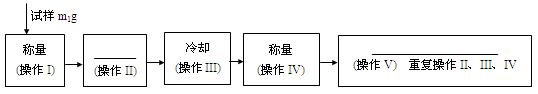
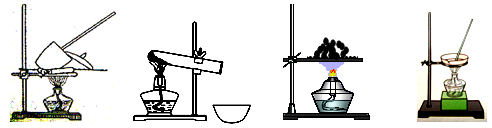
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验 | 解释或结论 |
| A | 用洁净的Pt丝蘸取某溶液进行焰色反应,火焰呈黄色 | 该溶液中一定含有Na+, 无K+ |
| B | 用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧 | CO2、H2O与Na2O2反应是放热反应 |
| C | 向溴水中滴入植物油,振荡后,油层显无色 | 溴不溶于油脂 |
| D | 将硫酸酸化的H2O2滴入Fe(NO3)2溶液,溶液变黄色 | H2O2的氧化性比Fe3+强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
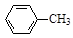 + 2KMnO4
+ 2KMnO4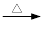
 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O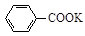 + HCl
+ HCl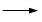
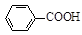 +KCl
+KCl
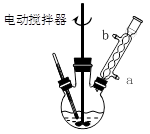
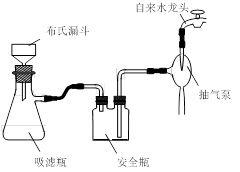
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 Na2S2O3(aq)
Na2S2O3(aq)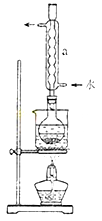
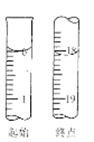
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
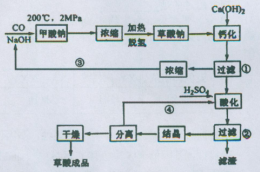
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com