
(1)图Ⅰ表示10mL量筒中液面的位置,A与B刻度间相差1mL,如果刻度A为4,量筒中液体的体积是________mL.
(2)图Ⅱ表示50mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)________.
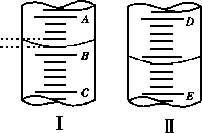
A、是amL
B、是(50-a)mL
C、一定大于amL
D、一定大于(50-a)mL
(3)能选用CCl4从碘水中萃取碘的原因是________.
(4)在中和热的测定实验中,取50mL0.50mol/L的盐酸,需加入下列________试剂(填序号).
①50mL0.50mol/LNaOH溶液②50mL0.55mol/LNaOH溶液③1.0gNaOH固体
(5)在硫酸铜晶体结晶水含量的测定实验中,若坩埚的质量为m,坩埚与硫酸铜晶体的质量为m1,加热后称量坩埚与无水硫酸铜的质量为m2,则晶体中结晶水的质量分数ω=________(写计算式).
科目:高中化学 来源: 题型:阅读理解
 【化学--选修3:物质结构与性质】
【化学--选修3:物质结构与性质】
| ||
| 2 |
| ||
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 下表列出了前20号元素中的某些元素性质的有关数据:
下表列出了前20号元素中的某些元素性质的有关数据:| 元素编号 元素性质 |
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径 (10-10m) |
1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | - |
| 最低价态 | - | - | -2 | - | -4 | -3 | -1 | - | -3 | -1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 下表列出了前20号元素中的某些元素性质的有关数据:
下表列出了前20号元素中的某些元素性质的有关数据:| 元素编号 元素性质 |
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径(10-10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | - |
| 最低价态 | - | - | -2 | - | -4 | -3 | -1 | - | -3 | -1 |
查看答案和解析>>
科目:高中化学 来源:2010年云南省昆明一中高三上学期第一次月考化学试题 题型:填空题
(8分)下表列出了前20号元素中的某些元素性质的有关数据:试回答下列问题:
(1)以上10种元素的原子中,最容易失电子的是 (填写元素符号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是 、 (写分子式)。某元素R的原子半径为1.02×10—10m,该元素在周期表中的位置是 ;若物质Na2R2是一种含有非极性共价键的离子化合物,请你写出该化合物的电子式 。
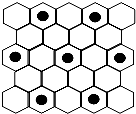
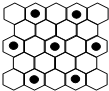
(3)元素⑤的某种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔融的②单质相互作用,形成某种青铜色的物质(其中“●”表示元素②的原子),右图为该物质部分原子分布示意图,请根据图找出原子排列规律并写出该物质的化学式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表列出了前20号元素中的某些元素性质的有关数据:试回答下列问题:
(1)以上10种元素的原子中,最容易失电子的是 (填写元素符号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是 、 (写分子式)。某元素R的原子半径为1.02×10—10m,该元素在周期表中的位置是 ;若物质Na2R2是一种含有非极性共价键的离子化合物,请你写出该化合物的电子式 。
(3)元素⑤的某种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔融的②单质相互作用,形成某种青铜色的物质(其中“●”表示元素②的原子),右图为该物质部分原子分布示意图,请根据图找出原子排列规律并写出该物质的化学式 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com