
下列溶液中有关微粒的物质的量浓度关系正确的是
A.3.0 L 0.1 mol·L-1 NaOH溶液中缓慢通入CO2至溶液增重8.8 g时,溶液中:
c(Na+)>c(CO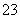 )>c(HCO
)>c(HCO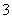 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B.常温下,将CH3COONa溶液和稀盐酸混合至溶液pH=7:
c(Na+)>c(CH3COO-)>c(Cl-)=c(CH3COOH)>c(H+)=c(OH-)
C.常温下,pH=6的NaHSO3溶液中:c(SO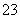 )-c(H2SO3)=9.9×10-7 mol·L-1
)-c(H2SO3)=9.9×10-7 mol·L-1
D.物质的量浓度之比为1∶2的NaClO、NaHCO3混合溶液中:
c(HClO)+c(ClO-)=2c(HCO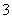 )+2c(H2CO3)+2c(CO
)+2c(H2CO3)+2c(CO )
)
科目:高中化学 来源: 题型:
室温下,将1mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为 △H2;CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s)
△H2;CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s) 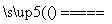 CuSO4(s)+5H2O(l), 热效应为△H3。则下列判断正确的是
CuSO4(s)+5H2O(l), 热效应为△H3。则下列判断正确的是
A.△H2>△H3 B.△H1<△H3
C.△H1+△H3 =△H2 D.△H1+△H2 >△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
等物质的量的镁和铝混合均匀后,分为等量的四份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是( )
|
| A. | 3 mol•L﹣1HCl溶液 | B. | 3 mol•L﹣1HNO3溶液 |
|
| C. | 8 mol•L﹣1NaOH溶液 | D. | 18 mol•L﹣1浓H2SO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质的性质和该性质的应用均正确的是
A.浓硫酸具有吸水性,可用于干燥氨气、二氧化碳等气体
B.二氧化硫具有漂白性,可用于加工食品使食品增白
C.铝具有良好的导电性,钢抗拉强度大,钢芯铝绞线可用作远距离高压输电线材料
D.铜的金属活动性比铁弱,可用铜罐代替铁罐贮运浓硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W的原子序数依次增大,X是形成化合物种类最多的元素,且X常见化合价为+1和-1,Y原子最外层电子数是次外层的3倍;Z与X处于同一主族,W的原子序数是Y的2倍。下列叙述不正确的是
A.原子半径的大小顺序:r(Z)>r(W)>r(Y)>r(X)
B.元素Y的简单气态氢化物的热稳定性比W的弱
C.化合物Z2Y2与X2Y反应时,Z2Y2既是氧化剂又是还原剂
D.由X、Y、Z、W四种元素组成的化合物其水溶液可能显酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术。反应①为主反应,反应②和③为副反应。
①1/4CaSO4(s)+CO(g)  1/4CaS(s)+CO2(g) ∆H1
1/4CaS(s)+CO2(g) ∆H1
②CaSO4(s)+CO(g)  CaO(s)+CO2(g) +SO2(g) ∆H2
CaO(s)+CO2(g) +SO2(g) ∆H2
③CO(g)  1/2C(s)+1/2CO2(g) ∆H3
1/2C(s)+1/2CO2(g) ∆H3
则反应2CaSO4(s)+7CO(g)  CaS(s)+CaO(s)+6CO2(g)+C(s) +SO2(g)的∆H=
CaS(s)+CaO(s)+6CO2(g)+C(s) +SO2(g)的∆H=
 (用∆H1、∆H2和∆H3表示)
(用∆H1、∆H2和∆H3表示)
(2)将燃煤废气中的CO2转化为二甲醚的反应原理为:
2CO2(g)+6H2(g)  CH3OCH3(g)+3H2O(g);ΔH
CH3OCH3(g)+3H2O(g);ΔH
①该反应平衡常数表达式为K= 。
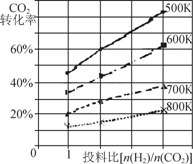
②已知在某压强下,该反应在不同温度、不同投料
比时,CO2的转化率如右图所示。该反应的ΔH
____(填“>”“<”或“=”)0。若温度不变,减
小反应投料比[n(H2) /n(CO2)],则K将 (填“增大”“减小”或“不变”)。
③二甲醚燃料电池具有启动快,效率高等优点,若电解质为酸性,二甲醚燃料电池的负极反应为 。
(3)一种以铜作催化剂脱硫有如下两个过程:
①在铜的作用下完成工业尾气中SO2的部分催化氧化,所发生反应为:
2SO2+2nCu+(n+1)O2+(2-2n) H2O=2nCuSO4+(2-2n) H2SO4
 从环境保护的角度看,催化脱硫的意义为
从环境保护的角度看,催化脱硫的意义为
。
②利用右图所示电化学装置吸收另一部分SO2,
并完成Cu的再生。写出装置内所发生反应的
总的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某校活动小组为探究金属腐蚀的相关原理,设计了如下图a所示装置,图a的铁棒末段分别连上一块Zn片和Cu片,并静置于含有K3Fe(CN)6及酚酞的混合凝胶上。一段时间后发现凝胶的某些区域(如下图b示)发生了变化,已知Fe2+可用K3Fe(CN)6来检验(呈蓝色)。则下列说法不正确的是( )

A.甲区呈现红色 B.乙区产生Zn2+
C.丙区发生的电极反应式:Cu-2e-= Cu2+ D.丁区呈现蓝色

查看答案和解析>>
科目:高中化学 来源: 题型:
合成尿素的反应是分作两步进行的:
① 2CO2(g)+ NH3(g)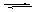 H2NCOONH4(aq)(氨基甲酸铵) △H =-159.47kJ/mol
H2NCOONH4(aq)(氨基甲酸铵) △H =-159.47kJ/mol
②H2NCOONH4(aq)CO(NH2)2(aq)+ H2O(l) △H =-28.49k J/mol
J/mol
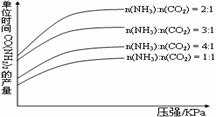
在生产条件下,单位时间内获得尿素的产量与压强和n(NH3):n(CO2)的关系如右图所示。生产过程中n(NH3):n(CO2)的最佳配比为 ,而实际实际生产条件下,往往使n(NH3):n(CO2)≥3,这是因为 。在得到的尿素溶液中会含有少量的氨基甲酸铵,除去这种杂质最简便的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
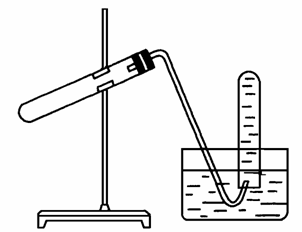
如右图装置可用于( )
A.用NH4Cl与浓NaOH溶液反应制NH3
B.用Cu与浓硝酸反应制NO2
C.用Cu与稀硝酸反应制NO
D.加热NaHCO3制CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com