
下列离子方程式正确的是( )
A.向Ca(HCO3)2溶液中加入过量NaOH溶液:
Ca2++HCO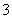 +OH-===CaCO3↓+H2O
+OH-===CaCO3↓+H2O
B.用石墨电极电解饱和食盐水:
2H++2Cl-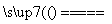 Cl2↑+H2↑
Cl2↑+H2↑
C.AlCl3溶液和过量氨水反应:
Al3++3OH-===Al(OH)3↓
D.向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置一段时间后变蓝:4H++4I-+O2===2I2+2H2O
科目:高中化学 来源: 题型:
碳的燃烧热为393.5 kJ/mol,下列热化学方程式正确的是
A.C(s)+O2(g)=CO2(g) △H = + 393.5 kJ/mol
B.C(s)+1/2O2(g)=CO(g) △H = - 393.5 kJ/mol
C.C + O2 = CO2 △H = - 393.5 kJ/mol
D.C(s)+O2(g)=CO2(g) △H = - 393.5 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )
A.高温下二氧化硅与碳酸钠反应放出二氧化碳,说明硅酸(H2SiO3)的酸性比碳酸强
B.陶瓷、玻璃、水泥容器都能贮存氢氟酸
C.石灰抹墙、水泥砌墙的硬化过程原理相同
D.玻璃窑中出来的气体的主要成分是二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废旧黄铜(Cu、Zn合金,含少量杂质Fe)制备胆矾晶体(CuSO4·5H2O)及副产物ZnO。制备流程图如下:
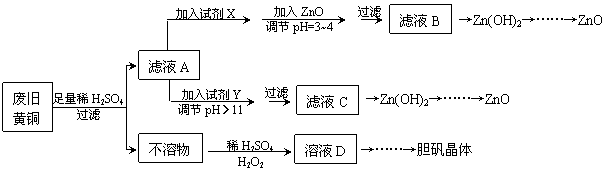

已知:Zn及化合物的性质与Al及化合物的性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)。
| Fe3+ | Fe2+ | Zn2+ | |
| 开始沉淀的pH | 1.1 | 5.8 | 5.9 |
| 沉淀完全的pH | 3.0 | 8.8 | 8.9 |
请回答下列问题:
⑴试剂X可能是__________,其作用是____________________。
⑵加入ZnO调节pH=3~4的目的是____________________。
⑶由不溶物生成溶液D的化学方程式为______________________________。
⑷由溶液D制胆矾晶体包含的主要操作步骤是______________________________。
⑸下列试剂可作为Y试剂的是______。
A.ZnO B.NaOH C.Na2CO3 D.ZnSO4
若在滤液C中逐滴加入盐酸直到过量,则产生的现象是______________________________。
⑹测定胆矾晶体的纯度(不含能与I-发生反应的氧化性杂质):准确称取0.5000g胆矾晶体置于锥形瓶中,加适量水溶解,再加入过量KI,用0.1000mol·L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液19.40mL。已知:上述滴定过程中的离子方程式如下:
2Cu2++4I- 2CuI(白色)↓+I2,I2+2S2O32-
2CuI(白色)↓+I2,I2+2S2O32- 2I-+S4O62-
2I-+S4O62-
①胆矾晶体的纯度为_______________。
②在滴定过程中剧烈摇动(溶液不外溅)锥形瓶,则所测得的纯度将会__________(填“偏高”、“偏低”
或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
若两物质恰好完全反应,则下列各项中反应前后一定保持不变的是( )
①电子总数 ②原子总数 ③分子总数 ④物质的总能量 ⑤物质的总质量
A.①②⑤ B.①③⑤
C.②③④ D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是( )
A.硫酸铝溶液中滴加过量浓氨水:Al3++4NH3·H2O===AlO +4NH
+4NH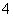 +2H2O
+2H2O
B.乙酸钠溶液显碱性的原因:CH3COO-+H2O===CH3COOH+OH-
C.氢氧化钠溶液吸收少量SO2气体:SO2+2OH-===SO +H2O
+H2O
D.漂白粉放置在空气中变质:ClO-+CO2+H2O===HClO+HCO
查看答案和解析>>
科目:高中化学 来源: 题型:
中学化学中几种常见物质的转化关系如图所示(图中部分反应物或生成物及反应条件未列出)。
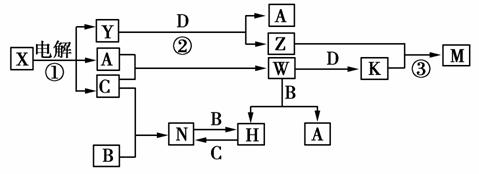
已知:A、B、C、D是单质,其余是化合物,其中B、D是常见金属,且组成B的元素属于过渡元素。又知A在C中点燃有苍白色火焰,M既可溶于盐酸又可溶于NaOH溶液。请回答下列问题:
(1)W的电子式是__________________。
(2)写出N的化学式:________,并任写一种N的主要用途:_____
_________________________________________________________。
(3)写出下列反应的离子方程式:
反应①_______________________________________________。
反应③_______________________________________________。
K溶液和过量氨水反应_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
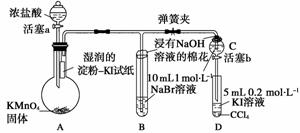
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其电子式是______________________________________。
(2)验证氯气的氧化性强于碘的实验现象是__________________________________。
(3)B中溶液发生反应的离子方程式是______________________________________。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是_________________________
________________________________________________________________________。
(5)过程Ⅲ实验的目的是_______________________ ___________________________。
___________________________。
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下____________________,得电子能力逐渐减弱。
查看答案和解析>>
科目:高中化学 来源: 题型:
如右图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )
A.产生气体的体积:①>②
B.①的溶液复原可向电解后的溶液中加氯化铜;②中电解后溶液的pH不变
C.电极上析出物质的质量:①>②
D.电极反应式:①中阳极2Cl- -2e- = Cl2↑
②中负极 2H+ + 2e- = H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com