
【题目】NH3和CO2是两种重要的化工原料。
(1)在一定温度下,在固定体积的密闭容器中发生反应:N2+3H22NH3。该可逆反应达到化学平衡的标志是_________(填字母)。
a.3v(H2)正=2v(NH3)逆
b.单位时间生成m mol N2的同时消耗3m mol H2
c.混合气体的密度不再随时间变化
d.a molN≡N键断裂的同时,有6a mol N-H键断裂
(2)最近科学家们研制成功一种新型催化剂,能将CO2转变为甲烷。在常压、300 ℃,CO2与H2体积比为1∶4时反应,CO2转化率达90%。
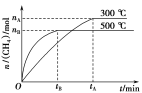
①此反应的化学方程式是_________。
②一定条件下,某兴趣小组,在体积为V L的密闭容器中,模拟此反应达到化学平衡状态。该反应的平衡常数表达式为_________;由上图可知升高温度,K将_________(填“增大”、“减小”或“不变”);300 ℃时,从反应开始,到达到平衡,以H2的浓度变化表示的化学反应速率是_________(用nA、tA、V表示)。
(3)一氧化碳能还原金属氧化物生成金属单质和二氧化碳。下图是四种金属氧化物(Cr2O3、SnO2、PbO2、Cu2O)被一氧化碳还原时lgc(CO)/c(CO2)与温度(T)的关系图。
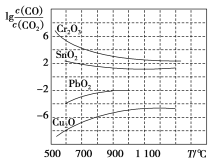
800 ℃时,四种金属氧化物中最易被一氧化碳还原的金属氧化物与CO反应的化学方程式为_________,该反应的平衡常数K=_________。
【答案】bd ![]()
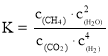 减小
减小 ![]()
![]()
![]()
【解析】
(1)可逆反应达到平衡状态的标志:![]() ,反应混合物中各组分的含量(质量分数、体积分数、物质的量分数)保持不变;
,反应混合物中各组分的含量(质量分数、体积分数、物质的量分数)保持不变;
(2)①在![]() 、新型催化剂的作用下,二氧化碳(
、新型催化剂的作用下,二氧化碳(![]() )与氢气(
)与氢气(![]() )反应生成甲烷(
)反应生成甲烷(![]() )和水(
)和水(![]() );
);
②根据化学平衡常数为生成物的浓度幂之积比反应物的浓度幂之积,列平衡常数的表达式;根据升高温度,平衡的移动,![]() 的变化判断平衡常数的变化,根据化学反应速率是
的变化判断平衡常数的变化,根据化学反应速率是![]() 计算;
计算;
(3)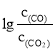 越小,K=
越小,K=![]() 越大,反应程度越大,所以最容易被还原的是
越大,反应程度越大,所以最容易被还原的是![]() 。
。
(1)a.化学反应速率之比等于化学计量数之比,![]() ,
,![]() ,a错误;
,a错误;
b.单位时间生成![]() 是逆反应,同时消耗
是逆反应,同时消耗![]() 是正反应,且,
是正反应,且,![]() ,
,![]() ,b正确;
,b正确;
c.![]() ,
,![]() 不变,
不变,![]() 不,所以
不,所以![]() 不再随时间变化,不能作为判断化学反应达到平衡的标志,c错误;
不再随时间变化,不能作为判断化学反应达到平衡的标志,c错误;
d.![]() 键断裂是正反应,同时
键断裂是正反应,同时![]() 键断裂是逆反应,
键断裂是逆反应,![]() ,
,![]() ,d正确。
,d正确。
(2)①300℃、新型催化剂的作用下,二氧化碳(![]() )与氢气(
)与氢气(![]() )反应生成甲烷(
)反应生成甲烷(![]() )和水(
)和水(![]() ),其化学反应方程式为:
),其化学反应方程式为:![]() ,
,
②化学平衡常数为生成物的浓度幂之积比反应物的浓度幂之积,其平衡常数的表达式为: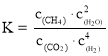 ,根据图可知,升高温度,
,根据图可知,升高温度,![]() 减少,平衡逆向移动,
减少,平衡逆向移动,![]() 减小;在
减小;在![]() 时,
时,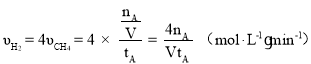 ;
;
(3)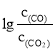 越小,K=
越小,K=![]() 越大,反应程度越大,所以最容易被还原的是
越大,反应程度越大,所以最容易被还原的是![]() ,其化学反应方程式为:
,其化学反应方程式为:![]() ,平衡常数表达式:
,平衡常数表达式:![]() ,
,![]() 时,
时,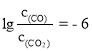 ,
,![]() =106。
=106。


科目:高中化学 来源: 题型:
【题目】A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中,A、C及B、D分别是同主族元素;A元素的原子半径是所有主族元素中原子半径最小的;B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的2倍;四种元素所形成的单质中A、B单质是气体,C、D单质是固体。
(1)写出以下元素的名称:B___;C___。
(2)写出D元素在周期表中的位置___。
(3)用电子式表示C2D的形成过程:___。
(4)写出由B、C两元素所形成的原子个数比为1:1的化合物的的电子式___;属于___(填“离子”或“共价”)化合物,存在的化学键的种类有___;写出它与水反应的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知烃A的分子式为C6H12,分子中含有碳碳双键,且仅有一种类型的氢原子,在下面的转化关系中,D1、D2互为同分异构体,E1、E2互为同分异构体。

(1)反应②的化学方程式为
___________________________________________________________;
(2)C的化学名称是_____________________________;E2的结构简式是_______________________;
(3)④、⑥的反应类型依次是_________________________、__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用通式为“![]() ”表示不同卤素之间靠共用电子对形成的卤素互化物
”表示不同卤素之间靠共用电子对形成的卤素互化物 ![]() 已知非金属性:
已知非金属性:![]() ,其化学性质和卤素单质相似。则下列说法中正确的是( )
,其化学性质和卤素单质相似。则下列说法中正确的是( )
A.ICl与水反应可生成 HCl 和 HIO,则1mol ICl 参加反应转移电子为 1mol
B.某温度下液态![]() 发生电离:
发生电离:![]() ,一定有c
,一定有c ![]()
![]()
![]()
C.BrCl与Mg反应生成![]() 和
和![]()
D.![]() 与卤素单质一样都是非极性分子
与卤素单质一样都是非极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸在溶剂中的电离是酸中的H+转移给溶剂分子,如:HCl+H2O=H3O++Cl-。已知H2SO4和HNO3在冰醋酸中的电离平衡常数Ka1(H2SO4)=6.3×10-9,Ka(HNO3)=4.2×10-10。下列说法正确的是( )
A.冰醋酸中H2SO4的电离方程式:H2SO4+2CH3COOH=SO42-+2CH3COOH2+
B. H2SO4的冰醋酸溶液中:c(CH3COOH2+)= c(HSO4-)+ 2c(SO42-)+ c(CH3COO-)
C.浓度均为0.1mol/L的H2SO4或HNO3的冰醋酸溶液:pH(H2SO4)>pH(HNO3)
D.向HNO3的冰醋酸溶液中加入冰醋酸,![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学一选修5:有机化学基础】
某高聚物W和树脂X的合成路线如下:
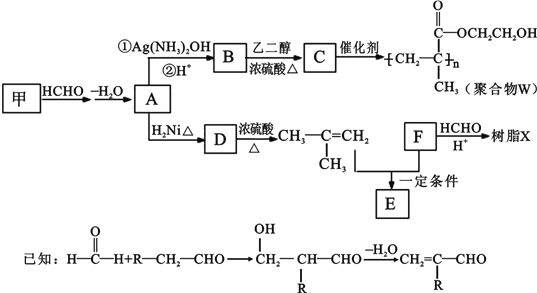
(1) A 的结构简式是_____。
(2) C中含氧官能团的名称是_____。
(3) D 的名称是_____。
(4) A→B 的第一步化学反应方程式是__
(5) 已知 F 的相对分子质量为 110,分子中碳原子、氢原子数都是氧原子数的 3 倍,苯环上的氢原子化学环境都相同,则 F 能发生的反应是(填字母)___。
a.加成反应 b.加聚反应 c.氧化反应 d.水解反应
(6) E 的分子式为 C10H14O2,含三个甲基,苯环上的一溴代物有两种。生成 E 的化学方程式是_____。
(7) B 有多种同分异构体。属于酯且含有碳碳双键的同分异构体共有__种(不考虑顺反异构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是生物体内四种有机物的组成与功能关系图,有关叙述错误的是
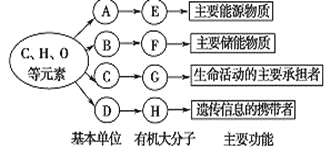
A. 小麦种子细胞中,物质A是葡萄糖,物质E是淀粉
B. 相同质量的E和F彻底氧化分解,释放能量较多的是F
C. 物质C的种类约有20种,基本组成元素是C、H、O、N
D. SARS病毒的物质H彻底水解后,产物是CO2和H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把1mol X气体和0.5mol Y气体混合于2L的密闭容器中,发生如下反应:
![]() ,2min末生成0.2mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol·L-1·min-1,试计算
,2min末生成0.2mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol·L-1·min-1,试计算
(1)前2min内,用X表示的平均反应速率____________。
(2)前2min内Y的转化率____________。
(3)化学方程式中Z的化学计量数n____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com