
����Ŀ���±�ΪԪ�����ڱ���һ���֣������Ԫ�آ٩����ڱ��е�λ�ã��û�ѧ����ش��������⣺
�� | IA | 0 | ||||||
1 | �� | ��A | ��A | ��A | ��A | ��A | ��A | |
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | �� | |||
��1��д�����ԭ�ӽṹʾ��ͼ ��
��2���ܡ��ݡ���ԭ�Ӱ뾶�ɴ�С��˳��Ϊ����Ԫ�ط��Żش𣩣�
��3���ڡ��ۡ��ߵ���ۺ������������ǿ����˳�������û�ѧʽ�ش�
��4����Ԫ�����γɵ��ʵĽṹʽΪ ��
��5���ĵ�����١�������Ԫ���γɻ������ˮ��Һ��Ӧ�����ӷ���ʽΪ�� ��
��6����Ԫ�����Ԫ���γɵĻ������У���ѧ������Ϊ
���𰸡�
��1��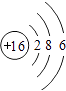
��2��Na��Al��O
��3��HNO3��H2CO3��H2SiO3
��4��N��N
��5��2Al+6H+=2Al3++3H2��
��6�����Ӽ�
���������⣺����Ԫ�������ڱ��е�λ�ÿ�֪����ΪH����ΪC����ΪN����ΪO����ΪNa����ΪAl����ΪSi����ΪS����ΪCl.
��1.��S��ԭ�ӽṹ����3�����Ӳ㣬����������Ϊ6��Sԭ�ӽṹʾ��ͼΪ 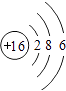 �����Դ��ǣ�
�����Դ��ǣ� 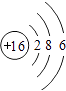 ��
��
��2.�����Ӳ�Խ�࣬ԭ�Ӱ뾶Խ��ͬ����ԭ���������ԭ�Ӱ뾶С���ܡ��ݡ���ԭ�Ӱ뾶�ɴ�С��˳��ΪNa��Al��O�����Դ��ǣ�Na��Al��O��
��3.���ǽ�����Խǿ����ۺ����������Խǿ����ڡ��ۡ��ߵ���ۺ������������ǿ����˳����HNO3��H2CO3��H2SiO3 �� ���Դ��ǣ�HNO3��H2CO3��H2SiO3��
��4.����Ԫ�����γɵ���Ϊ�������ṹʽΪN��N�����Դ��ǣ�N��N��
��5.��Al�����ᷴӦ�����Ȼ��������������ӷ�ӦΪ2Al+6H+=2Al3++3H2�������Դ��ǣ�2Al+6H+=2Al3++3H2����
��6.����Ԫ�����Ԫ���γɵĻ�����ΪNaCl��ֻ�����Ӽ������Դ��ǣ����Ӽ���


 ���ɶ���ܲ��¿�ֱͨ�п�ϵ�д�
���ɶ���ܲ��¿�ֱͨ�п�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з���������ԭ�Ӷ����������Ϊ8���ӽṹ����
A. BF3 B. PCl5 C. NH3 D. CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ����Ҫ����������������Ҫ�ɷ�ΪAl2O3 �� Fe2O3��SiO2�ȣ���ұ��Al�Ĺ�ҵ������������ͼ�� 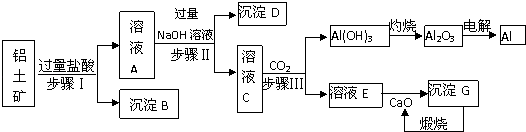
��1����ҺA�к�����������Ҫ�� ��
��2��д������II������ҺC �����ӷ���ʽ ��
����I��II��III��Ҫ�õ��ķ��뷽���� ��
��3�����������У���CaO����ѭ��ʹ���⣬������ѭ��ʹ�õ����������ѧʽ����
��4�����������������������Ļ�����γ����ȼ��������ȷ�Ӧ���Ӹֹ죨��ʾ����Ӧ�������������ʣ����������������ڸ����·�����Ӧ�Ļ�ѧ����ʽΪ��
.
��5����������a�����������ұ����b�ֵ������������������������ģ�����ԭ��������Al2O3�Ĵ��ȣ��������������ú�a��b�����ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йؾ����������ȷ����
A.�������庬�н��������Ӻ����ɵ���
B.ԭ�Ӿ���һ���ǵ���
C.���Ӿ���һ���ǻ�����
D.���������Ӳ��>ԭ�Ӿ����Ӳ��>���Ӿ����Ӳ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵��������ǣ� ��
A.���й��ۼ��Ļ������ǹ��ۻ�����
B.���м��Լ��ķ��ӿ����ǷǼ��Է���
C.�е���ת�Ƶķ�Ӧ��������ԭ��Ӧ
D.ˮ��Һ������ȫ����ĵ������ǿ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��̲����ڵ��Ĺ̶�����
A. ����ʱ�����е��������������
B. ��NH3�Ʊ�NH4Cl
C. ��N2��H2�ϳɰ�
D. ����ֲ��ĸ������Ѵ����еĵ�ת���ɰ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A. ���ӻ�������ֻ�ܺ����Ӽ��������й��ۼ�
B. �ǽ���Ԫ��֮���γɵĻ�ѧ��һ���ǹ��ۼ�
C. ��������ͬ��������һ����ͬһԪ��
D. ��ѧ�����ƻ��ı仯��һ���ǻ�ѧ�仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������NaOH��Na2CO3��Ba(OH)2������Һ�����ѡ�������Լ��е�( )
A. ʯ����Һ B. ϡ���� C. ����ʯ��ˮ D. CaCl2��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����š�3px��û�и�������Ϣ�ǣ�������
A. ���Ӳ�B. �����Dz�C. �������ڿռ����չ����D. ���ӵ���������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com