
【题目】主族元素A、B、C、D的原子序数依次增加。甲、丙、戊是由这些元素组成的二元化合物,丙分子中原子个数比为1:1,乙是元素D的单质,通常为深红棕色液体,丁为淡黄色固体,0.01 mol/L戊溶液的pH为2,己为难溶于水、密度比水大的油状物。上述物质的转化关系如图所示。下列说法中不正确的是
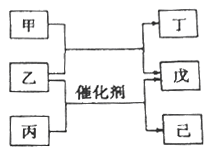
A. 四种元素既不同周期也不同主族
B. 元素的非金属性A<B<C
C. 丙常温常压下为气态
D. C的最高价氧化物对应的水化物为强酸
【答案】C
【解析】主族元素A、B、C、D的原子序数依次增加。甲、丙、戊是由这些元素组成的二元化合物,丙分子中原子个数比为1:1,乙是元素D的单质,通常为深红棕色液体,乙为溴,D为Br元素; 0.01molL-1戊溶液的pH为2,则戊为HBr,丁为淡黄色固体,则丁为S,则甲为H2S,己为难溶于水、密度比水大的油状物,根据框图,乙与丙在催化剂作用下发生取代反应,则己为溴苯,丙为苯,则A、B、C、D分别为H、C、S、Br。A.根据上述分析, 四种元素既不同周期也不同主族,故A正确;B. 根据题周期,从左到右,元素的非金属性逐渐增强,题意主族,从上到下,元素的非金属性逐渐减弱,元素的非金属性A<B<C,故B正确;C. 丙为苯,常温常压下为液态,故C错误;D. C为S元素,硫酸为强酸,故D正确;故选C。


科目:高中化学 来源: 题型:
【题目】下列有关物质的性质和应用都正确的是( )
A.MgO、Al2O3熔点高,都可用于制作耐火材料
B.氨气显碱性,可用碱石灰或无水CaCl2干燥
C.氢氟酸具有强酸性,可用于雕刻玻璃
D.铜的活动性比铁弱,可在海轮外壳上装铜块以减缓海轮腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用A、B、C三个装置都可以制取溴苯,其中A是最基本的制备装置,B、C是改进后的装置,请仔细分析、对比三套装置,然后回答以下问题:

(1)写出三个装置中都发生的发应的化学方程式:__________、___________。
(2)装置A和C中均采用了长玻璃导管,其作用是_____________________________。
(3)装置B和C较好地解决了装置A中存在的加药品和及时密封的矛盾,方便了操作。装置A中这一问题在实验中易造成的不良后果是________________________________。
(4)装置B中采用了洗气瓶吸收装置,其作用是_______________________。
(5)装置B中也存在两个明显的缺点,使实验的效果不好或不能正常进行。这两个缺点是
___________________________、________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,a中放置附着氧化铜粉未的石棉绒,向a中持续通入气态物质X,可以观察到石棉绒上黒色粉末变成红色固态物质,同时c处的U型管中有无色液体生成,(假设X气体全部反应,各处反应均完全)

(1)X可能是_________(填字母)。
A.H2 B.CO C.H2和CO D.CH3CH2OH蒸气
(2)写出a处反应的化学方程式:________________;
(3)c处液体主要成分的结构简式为___________,检验该物质的操作步骤是_____________;
其现象为__________;有关的化学方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图1是某化学兴趣小组进行丁烷裂解的实验流程.(注:CuO能将烃氧化成CO2和H2O,G后面装置与答题无关,铁架台等已省略.)按下图连好装置后,需进行的实验操作有:①给D、G装置加热;②检查整套装置的气密性;③排出装置中的空气等…
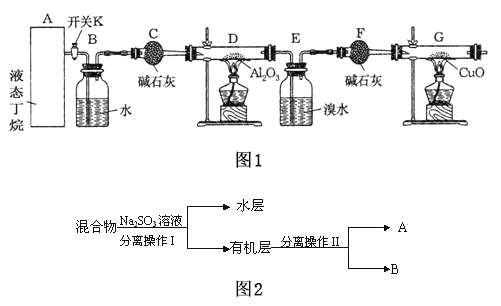
(1)这三步操作的先后顺序依次是_________________;
(2)B装置所起的作用是________________;
(3)假定丁烷按C4H10→C2H6+C2H4和C4H10→CH4+C3H6的方式完全裂解,当(E+F)装置的总质量比反应前增加了0.7g,G装置的质量减少了1.76g,则丁烷的裂解产物中,甲烷与乙烷的物质的量之比为 ____________________(假定流经D、G装置中的气体能完全反应)。
(4)若对E装置中的混合物再按图2流程实验:
①分离操作Ⅰ和Ⅱ的名称分别是:Ⅰ ______________,分液Ⅱ_____________;
Na2SO3溶液的作用是____________(用离子方程式表示)。
②已知B的碳原子数大于A的碳原子数,请写出B的结构简式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辉铜矿是铜矿的主要品种之一传统的火法冶炼在资源的综合利用、环境保护等方面会遇到困难。辉铜矿的湿法冶炼目前国内外都处于探索阶段。自氧化还氨氮分离法是一种较为理想的湿法冶炼方法,工艺流程如下图所示:
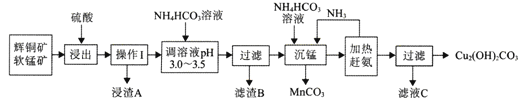
已知:
① 辉铜矿的主要成分是Cu2S,含有较多的Fe2O3、SiO2等。
② 软锰矿的主要成分是MnO2,含有较多的SiO2等。
③ 浸出时,生成一种非金属单质。
④ 室温下,Kap[Fe(OH)3]=4.0×10-38mol/L,Kap[Fe(OH)2]=8.0×10-16mol/L
完成下列填空:
(l)浸出前需要先将矿石粉碎,其目的是__________。
(2)写山浸出时主要反应的离子方程式_____________。
(3)浸渣A的主要成分为_______;调溶液pH 3.0-3.5的目的是除去______离子;室温下,若该离子的浓度为4.0×10-8mol/L,则溶液的pH=__________。
(4) 工业上可将MnCO3、在300℃左右氧化来制取具有较好催化性能的MnO2,则MnCO3在空气中受热制取MnO2的化学方程式为_________________。
(5)从滤液C中提取硫酸氨晶体的步骤为_______、_______、过滤、洗涤、干操。
(6)与火法冶炼辉铜矿相比,用图中方法冶炼辉铜矿的优点有________、_____。(列举其中2条)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(11分)物质H俗称衣康酸,是制备高效粘合剂等多种精细化学品的重要原料,可经下列反应路线得到:
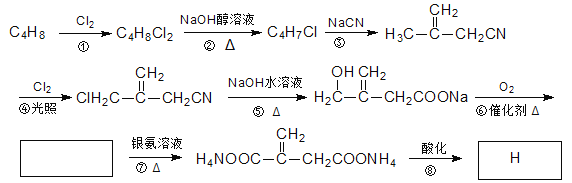
回答下列问题:
(1)C4H8的名称(系统命名)是 。
(2)反应⑥的化学方程式为 。
(3)衣康酸有多种同分异构体,其中与衣康酸属于同类且核磁共振氢谱有5个峰的有机物结构简式为 。
(4)下列关于H的说法正确的是 (填字母)
a.能使酸性KMnO4溶液或溴的CCl4溶液褪色
b.能与Na2CO3反应,但不与HBr反应
c.能与新制Cu(OH)2反应
d.1molH完全燃烧消耗5molO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com