
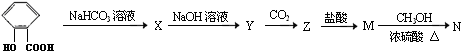
 Y
Y M
M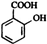 N
N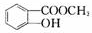
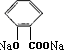 +CO2+H2O→
+CO2+H2O→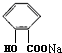 +NaHCO3.
+NaHCO3. 分析 酸性HCl>-COOH>H2CO3>C6H5OH>HCO3-; 中加入碳酸氢钠溶液,因酸性C6H5OH>HCO3-,酚羟基与碳酸氢根离子不反应,但-COOH>H2CO3,羧酸与碳酸氢根离子反应,所以X为
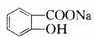
中加入碳酸氢钠溶液,因酸性C6H5OH>HCO3-,酚羟基与碳酸氢根离子不反应,但-COOH>H2CO3,羧酸与碳酸氢根离子反应,所以X为 ,酚羟基具有酸性,能和氢氧化钠反应,生成酚钠盐,所以Y为
,酚羟基具有酸性,能和氢氧化钠反应,生成酚钠盐,所以Y为 ,通入二氧化碳,碳酸性比苯酚的酸性强,二氧化碳和酚钠反应生成酚,所以Z为
,通入二氧化碳,碳酸性比苯酚的酸性强,二氧化碳和酚钠反应生成酚,所以Z为 ,酸性HCl>-COOH,加入盐酸,羧酸盐变成羧酸,所以M为
,酸性HCl>-COOH,加入盐酸,羧酸盐变成羧酸,所以M为 ,羧酸和醇发生酯化反应,所以N为
,羧酸和醇发生酯化反应,所以N为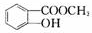 ,据此分析解答.
,据此分析解答.
解答 解:酸性HCl>-COOH>H2CO3>C6H5OH>HCO3-; 中加入碳酸氢钠溶液,因酸性C6H5OH>HCO3-,酚羟基与碳酸氢根离子不反应,但-COOH>H2CO3,羧酸与碳酸氢根离子反应,所以X为
中加入碳酸氢钠溶液,因酸性C6H5OH>HCO3-,酚羟基与碳酸氢根离子不反应,但-COOH>H2CO3,羧酸与碳酸氢根离子反应,所以X为 ,酚羟基具有酸性,能和氢氧化钠反应,生成酚钠盐,所以Y为
,酚羟基具有酸性,能和氢氧化钠反应,生成酚钠盐,所以Y为 ,通入二氧化碳,碳酸性比苯酚的酸性强,二氧化碳和酚钠反应生成酚,所以Z为
,通入二氧化碳,碳酸性比苯酚的酸性强,二氧化碳和酚钠反应生成酚,所以Z为 ,酸性HCl>-COOH,加入盐酸,羧酸盐变成羧酸,所以M为
,酸性HCl>-COOH,加入盐酸,羧酸盐变成羧酸,所以M为 ,羧酸和醇发生酯化反应,所以N为
,羧酸和醇发生酯化反应,所以N为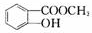 ,
,
(1)根据上面的分析可知,X为 ,Y为
,Y为 ,M为
,M为 ,N为
,N为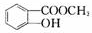 ,
,
故答案为: ;
; ;
; ;
;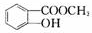 ;
;
(2)Y→Z化学方程式为 +CO2+H2O→
+CO2+H2O→ +NaHCO3,
+NaHCO3,
故答案为: +CO2+H2O→
+CO2+H2O→ +NaHCO3.
+NaHCO3.
点评 本题考查有机物的推断,涉及酚、醇、羧酸、酯等的性质与转化等,根据羧酸、酚羟基的性质利用题干信息顺推法进行判断,注意对常见官能团的理解掌握,题目难度中等.


 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⅦA族元素形成的单质的熔点随元素原子序数增大而升高 | |
| B. | ⅦA族元素易形成-1价离子 | |
| C. | 最高价氧化物的水化物显酸性 | |
| D. | 从上到下气态氢化物的稳定性依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 前者大 | B. | 后者大 | C. | 一样大 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A. | X、Y元素的最高价氧化物对应的水化物的碱性:Y比X弱 | |
| B. | 一定条件下,Z单质与W的常见单质直接生成ZW2 | |
| C. | Y的最高价氧化物对应的水化物能溶于浓氨水 | |
| D. | 一定条件下,X单质可以将W单质从其氢化物中置换出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是某同学设计的放热反应的观察装置,其实验操作是:
如图是某同学设计的放热反应的观察装置,其实验操作是:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
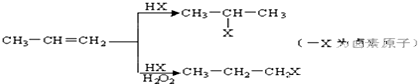
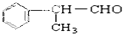 的物质,它是一种香料.
的物质,它是一种香料.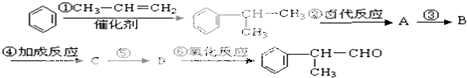
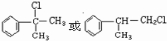 .
.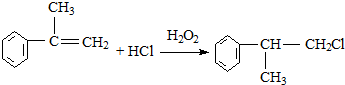 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定为2 | B. | 一定为3 | C. | 为2或3 | D. | 可以为任意数字 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com