
Ϊ̽��ij��̼�Ͻ���Ũ�����ڼ��������µķ�Ӧ�IJ��ֲ��ﲢ�ⶨ��̼�Ͻ�����Ԫ�ص�����������ij��ѧ�С���������ͼ��ʾ��ʵ��װ�ã����������ʵ��̽����




��1����Բ����ƿ�м���m g��̼�Ͻ𣬲��������Ũ���ᣬδ��ȼ�ƾ���ǰ��A��B��������������ԭ���ǣ��ٳ����£�Fe��Ũ�����жۻ����� ��
��2����Ӧһ��ʱ���A���ݳ������������Ȼ�Ͽ죬����Ӧ�¶Ƚϸ��⣬�����ܵ�ԭ���� ��
��3��װ��B�������� ��
��4����ͬѧ�۲쵽װ��C���а�ɫ�������ɣ����ó���ʹ����ʯ��ˮ����ǵ������Ƕ�����̼��
װ��A���ܲ���������̼�Ļ�ѧ����ʽΪ ��
��5����ͬѧ��Ϊ��ͬѧ�Ľ����Ǵ���ģ�����ΪΪ��ȷ�϶�����̼�Ĵ��ڣ�����װ��B-C֮������װ��M��װ��E��F��ʢ�ŵ��Լ��ֱ��� �� ��
����ʵ���۲쵽װ��F�е������� ��
��6����Щͬѧ��Ϊ�Ͻ�����Ԫ�ص�������������KMnO4��Һ���ⶨ��
��5Fe2+ + MnO4��+ 8H+ ==5Fe3+ + Mn2+ + 4H2O����
�ⶨ��Ԫ������������ʵ�鲽�����£�
I������ƿA�м�������Ļ�ԭ��ʹ��Һ�е�Fe3+��ȫת��ΪFe2+�����ˣ��õ���ҺB��
II������ҺBϡ��Ϊ250 mL��
III��ȡϡ��Һ25.00 mL����Ũ��Ϊc mol��L��1������KMnO4��Һ�ζ������εζ�ʵ������KMnO4��Һ�����ƽ��ֵΪV mL��
�ٲ�����У�����ҺBϡ��Ϊ250 mL��Ҫ�õ��IJ����������ձ�������������ͷ�ι��⣬������Ҫ�õ����� ��
�ڱ�ͬѧ��������еζ���ʽ���г�����ʡ�ԣ������������ ��������ĸ��ţ�

�۵ζ������� �����Ҫ������Ҫ��������ָʾ��������Ҫ��Ӧ�����ָʾ���� ��
����̼�Ͻ�����Ԫ�ص���������Ϊ ��
��15�֣���1��������̼��Ũ�����Ӧ��1�֣�
��2����̼������Һ���γ�ԭ��أ�1�֣�
��3������SO2�Ĵ��ڣ�1�֣�
��4��C + 2H2SO4 (Ũ) CO2��+
2SO2�� + 2H2O��3�֣�
CO2��+
2SO2�� + 2H2O��3�֣�
��5������KMnO4��Һ����ˮ�������������𰸣���Ʒ����Һ����1�֣���2�֣�
Ʒ����Һ����ɫ������������1�֣�
��6����250mL����ƿ��1�֣�
��b��1�֣�
�۲���Ҫ��1�֣�
��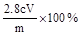 ��3�֣�
��3�֣�
��������
�����������1����̼�Ͻ�������̼���ʣ������£�����Ũ����ۻ���̼��Ũ�����Ӧ���������������2�������¶ȣ���ѧ��Ӧ���ʼӿ죻��̼������Һ���γ�ԭ��أ���ѧ��Ӧ����Ҳ��ӿ죻��3��װ��B��Ʒ����Һ���Լ��鷴Ӧ�������Ƿ����SO2����4��װ��A�в���CO2�ķ�ӦʽΪC + 2H2SO4
(Ũ)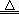 CO2��+
2SO2�� + 2H2O����5������CO2��SO2����ʹ����ʯ��ˮ����ǣ�����CO2ǰ�����ȥSO2������SO2�Ƿ����������SO2���л�ԭ�Ժ�Ư���ԣ���E��F�зֱ�ʢ�����������Ը��������Һ����ˮ�ȡ�Ʒ����Һ��F��Ʒ����Һ����ɫ�������Ա仯��C�б���ǣ�˵��A�з�Ӧ���ﺬ��CO2����6��������250mL��Һ��Ҫʹ��250mL����ƿ�������Ը��������Һ�ܸ�ʴ����a�������Ը��������Һ���ܲ�������b��ȷ��������Һ�ܸ�ʴ����c�������Ը��������Һ��������������ָʾ������˵ζ�ʱ����Ҫָʾ������c•V��֪��n(MnO4��)=c•V��10��3mol����5Fe2+ +
MnO4��+ 8H+ ==5Fe3+ + Mn2+
+ 4H2O��֪��n(Fe2+ )=5c•V��10��3mol����ϡ�Ͷ��ɿ�֪����ҺB��n(Fe2+ )=
CO2��+
2SO2�� + 2H2O����5������CO2��SO2����ʹ����ʯ��ˮ����ǣ�����CO2ǰ�����ȥSO2������SO2�Ƿ����������SO2���л�ԭ�Ժ�Ư���ԣ���E��F�зֱ�ʢ�����������Ը��������Һ����ˮ�ȡ�Ʒ����Һ��F��Ʒ����Һ����ɫ�������Ա仯��C�б���ǣ�˵��A�з�Ӧ���ﺬ��CO2����6��������250mL��Һ��Ҫʹ��250mL����ƿ�������Ը��������Һ�ܸ�ʴ����a�������Ը��������Һ���ܲ�������b��ȷ��������Һ�ܸ�ʴ����c�������Ը��������Һ��������������ָʾ������˵ζ�ʱ����Ҫָʾ������c•V��֪��n(MnO4��)=c•V��10��3mol����5Fe2+ +
MnO4��+ 8H+ ==5Fe3+ + Mn2+
+ 4H2O��֪��n(Fe2+ )=5c•V��10��3mol����ϡ�Ͷ��ɿ�֪����ҺB��n(Fe2+ )= ��5c•V��10��3mol������Ԫ���غ㡢n•M��֪�����Ͻ���m(Fe)=
��5c•V��10��3mol������Ԫ���غ㡢n•M��֪�����Ͻ���m(Fe)= ��5c•V��10��3��56g������̼�Ͻ�����Ԫ�ص���������Ϊ
��5c•V��10��3��56g������̼�Ͻ�����Ԫ�ص���������Ϊ ��5c•V��10��3��56/m��100%=
��5c•V��10��3��56/m��100%=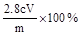 ��
��
���㣺�������仯�������Ҫ���ʡ�Ӱ�컯ѧ��Ӧ���ʵ����ء�SO2��CO2�ļ��顢������Һ���ζ�ԭ������Ʒ��ɵIJⶨ�����֪ʶ��


 Сѧ�̲�ȫ��ϵ�д�
Сѧ�̲�ȫ��ϵ�д� Сѧ��ѧ������ѿڶ���ϵ�д�
Сѧ��ѧ������ѿڶ���ϵ�д� ������Ӧ�������������ϵ�д�
������Ӧ�������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ||
| ||
| ||
| ||
| 11m-3b |
| 11m |
| 11m-3b |
| 11m |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
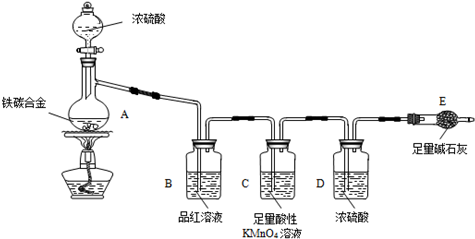
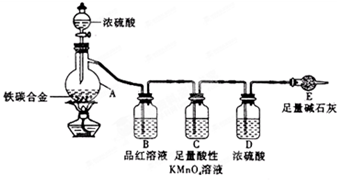 ij��ѧ��ȤС��Ϊ�˲ⶨij��̼�Ͻ�������������������̽��Ũ�����ijЩ���ʣ��������ͼ��ʾ��ʵ��װ�ú�ʵ�鷽�����г�������ʡ�ԣ�����ݴ���ش���Ӧ���⣮
ij��ѧ��ȤС��Ϊ�˲ⶨij��̼�Ͻ�������������������̽��Ũ�����ijЩ���ʣ��������ͼ��ʾ��ʵ��װ�ú�ʵ�鷽�����г�������ʡ�ԣ�����ݴ���ش���Ӧ���⣮| �� |
| ||
| ||
| 3b |
| 11a |
| 3b |
| 11a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
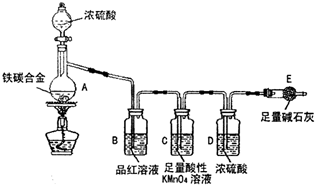 ij��ѧ��ȤС��Ϊ�˲ⶨij��̼�Ͻ𣨿�������̼���ֵ��ʵĻ���������������������̽��Ũ�����ijЩ���ʣ��������ͼ��ʾ��װ�ã��г�������ʡ�ԣ��ͷ�������ʵ�飮
ij��ѧ��ȤС��Ϊ�˲ⶨij��̼�Ͻ𣨿�������̼���ֵ��ʵĻ���������������������̽��Ũ�����ijЩ���ʣ��������ͼ��ʾ��װ�ã��г�������ʡ�ԣ��ͷ�������ʵ�飮�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com