
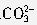 、
、 和Ca2+恰好完全形成了CaCO3沉淀。若将反应后的溶液在低温下加热蒸干,将所得固体冷却至室温称其质量为32.0g。
和Ca2+恰好完全形成了CaCO3沉淀。若将反应后的溶液在低温下加热蒸干,将所得固体冷却至室温称其质量为32.0g。 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 滴加溶液A的体积/mL | 10.0 | 20.0 | 30.0 |
| 生成气体的体积/mL(标准状况) | 89.6 | 179.2 | 224 |
| 16n(H2O2) |
| m(样品) |
查看答案和解析>>
科目:高中化学 来源:2014届福建省福州八县市高三上学期期中联考化学试卷(解析版) 题型:选择题
将11.9g由Mg、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了2.7g。另取等质量的合金溶于过量稀硝酸中,生成了6.72LNO(标准状况下),向反应后的溶液中加入适量NaOH溶液恰好使Mg2+、Al3+、Fe3+完全转化为沉淀,则沉淀的质量为
A.22.1g B.27.2g C.30g D.30.2g
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com