
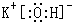 (填写电子式);
(填写电子式);分析 A、B、C、D和E都是元素周期表中前20号的元素,它们的原子序数依次增大,B、C、D元素的基态原子具有相同的能层数,处于同一周期,B、D元素的原子的p能级上都有1个未成对电子,价层电子排布为ns2np1或ns2np5,D原子得一个电子填入3p轨道后,3p轨道已充满,故D为Cl元素,B为Al元素,C原子的p轨道中有3个未成对电子,价层电子排布为3s23p3,故C为P元素;E是同周期第一电离能最小的元素,处于第ⅠA族,原子序数最大,故E处于第四周期,为K元素,A原子的价电子层的p轨道中只有1个电子,价层电子排布为ns2np1,处于第ⅢA族,原子序数最小,故A为B元素.
解答 解:A、B、C、D和E都是元素周期表中前20号的元素,它们的原子序数依次增大,B、C、D元素的基态原子具有相同的能层数,处于同一周期,B、D元素的原子的p能级上都有1个未成对电子,价层电子排布为ns2np1或ns2np5,D原子得一个电子填入3p轨道后,3p轨道已充满,故D为Cl元素,B为Al元素,C原子的p轨道中有3个未成对电子,价层电子排布为3s23p3,故C为P元素;E是同周期第一电离能最小的元素,处于第ⅠA族,原子序数最大,故E处于第四周期,为K元素,A原子的价电子层的p轨道中只有1个电子,价层电子排布为ns2np1,处于第ⅢA族,原子序数最小,故A为B元素,则
(1)由上述分析可知,A为B元素,B为Al元素,C为P元素,
故答案为:B、Al、P;
(2)五种元素中Cl元素非金属性最强,最高价氧化物对应水化物酸性最强的是HClO4,K元素的金属性最强,故KOH碱性最强,电子式为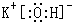 ,
,
故答案为:HClO4,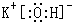 ;
;
(3)同周期自左而右,第一电离能增大,电负性增大,故第三周期中第一电离能最大的元素是Cl,电负性最大的元素是Cl,
故答案为:Cl;Cl;
(4)在BCl3分子中B原子成3个σ键,没有孤对电子,杂化轨道数目为3,采取sp2杂化,分子空间构型为平面三角形,
故答案为:sp2;平面三角形;
(5)Al与KOH反应的离子方程式为:2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑,
故答案为:2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑.
点评 考查元素推断、常用化学用语书写、元素周期律、杂化轨道与物质结构等,难度中等,注重物质结构的基础知识的考查.


科目:高中化学 来源: 题型:解答题
| 未成对电子数 | 电负性 | 气态氢化物稳定性 | 酸性 |
| N>O | C<N | H2S<H2O | H2SO4<HClO4 |
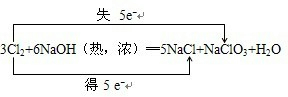 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④⑤⑩ | B. | ⑥①⑤③ | C. | ⑨②⑧① | D. | ⑦①③⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
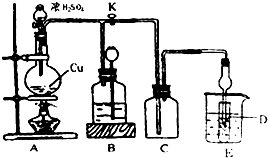
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | A的初$\frac{始浓度}{mol•{L}^{-1}}$ | B的初$\frac{始浓度}{mol•{L}^{-1}}$ | 生成C的$\frac{初始速率}{mol•{L}^{-1}•{s}^{-1}}$ |
| 1 | 1.0 | 1.0 | 1.2×10-2 |
| 2 | 2.0 | 1.0 | 2.4×10-2 |
| 3 | 4.0 | 1.0 | 4.9×10-2 |
| 4 | 1.0 | 1.0 | 1.2×10-2 |
| 5 | 1.0 | 2.0 | 4.8×10-2 |
| 6 | 1.0 | 4.0 | 1.9×10-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn为正极 | B. | 负极反应式:O2+4H++4e-→2H2O | ||
| C. | 正极发生氧化反应 | D. | 电解液肯定不是强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能/kJ•mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
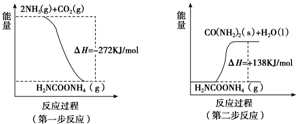
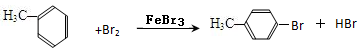 或
或
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com