
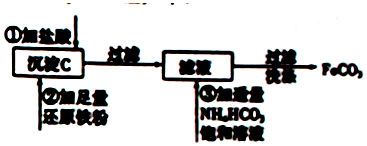
分析 ①沉淀C应为氢氧化铁,氢氧化铁加入盐酸生成氯化铁和水,氯化铁中加入铁粉生成氯化亚铁;
②过滤后溶液中含有亚铁离子,与碳酸氢根反应生成碳酸亚铁.
解答 解:①氢氧化铁加入盐酸生成氯化铁和水,离子方程式为Fe(OH)3+3H+=Fe3++3H2O,故答案为:Fe(OH)3+3H+=Fe3++3H2O;
②亚铁离子与碳酸氢根发生双水解反应Fe2++2HCO3-=FeCO3↓+CO2↑+H2O,故答案为:Fe2++2HCO3-=FeCO3↓+CO2↑+H2O.
点评 本题考查了制备方案的设计,题目难度中等,涉及化学方程式书写,明确实验目的、实验原理为解答关键,试题培养了学生的分析、理解能力.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对甲苯酚和苯甲醇 | B. | 甲酸甲酯和甲醛 | ||
| C. | 苯和乙烯 | D. | CH3CH2OH和CH3CH2CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 纯净物 | 混合物 | 电解质 | 非电解质 |
| A | 盐酸 | 水煤气 | 硫酸 | 干冰 |
| B | 蒸馏水 | 蔗糖溶液 | 氧化铝 | 二氧化硫 |
| C | 胆矾 | 氢氧化铁胶体 | 铁 | 碳酸钙 |
| D | 水银 | 澄清石灰水 | 氯化铜 | 碳酸钠 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 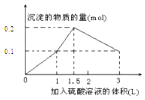 | B. | 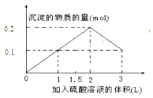 | ||
| C. | 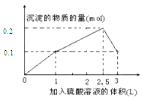 | D. | 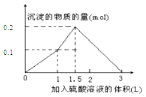 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 用标签所示浓盐酸配制250mL 0.4mol/L的稀盐酸,并进行有关实验.请回答:
用标签所示浓盐酸配制250mL 0.4mol/L的稀盐酸,并进行有关实验.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com