
发射卫星时可用肼(N2H4)作燃料.已知在298 K时,1 g肼气体燃烧生成氮气和水蒸气,放出16.7 kJ的热量.观察并分析下列肼燃烧反应的热化学方程式,判断这些热化学方程式是否正确.总结书写热化学方程式的原则,将你的思考与同学交流讨论.
(1)N2H4(g)+O2(g)![]() N2(g)+2H2O(g);ΔH=-534.4 kJ·mol-1
N2(g)+2H2O(g);ΔH=-534.4 kJ·mol-1
(2)N2H4(g)+O2(g)![]() N2(g)+2H2O(g);ΔH=+534.4 kJ·mol-1
N2(g)+2H2O(g);ΔH=+534.4 kJ·mol-1
(3)N2H4(g)+O2(g)![]() N2(g)+2H2O(l);ΔH=-534.4 kJ·mol-1
N2(g)+2H2O(l);ΔH=-534.4 kJ·mol-1
(4)N2H4+O2![]() N2+2H2O;ΔH=-534.4 kJ·mol-1
N2+2H2O;ΔH=-534.4 kJ·mol-1
(5)0.5N2H4(g)+0.5O2(g)![]() 0.5N2(g)+H2O(g);ΔH=-267.2 kJ·mol-1
0.5N2(g)+H2O(g);ΔH=-267.2 kJ·mol-1
科目:高中化学 来源: 题型:
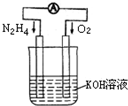 运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.| 10-9 |
| a-0.01 |
| 10-9 |
| a-0.01 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com