
【题目】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)B在周期表中的位置为第________周期第________族。
(2)E元素形成的氧化物对应的水化物的化学式为________________________。
(3)元素C、D、E形成的简单离子半径大小关系是______>________>________(用离子符号表示)。
(4)用电子式表示化合物D2C的形成过程:____________________。C、D还可形成化合物D2C2,D2C2中含有的化学键是_________________________。
(5)由A、B、C三种元素形成的离子化合物的化学式为__________________,它与强碱溶液共热,发生反应的离子方程式是______________________。
(6)某一反应体系中含有D2E、D2EC3、D2EC4三种物质,若此反应为分解反应,则此反应的化学方程式为________________________(化学式用具体的元素符号表示)。
【答案】(1)二 ⅤA (2)H2SO3、H2SO4
(3)S2- O2- Na+
(4)![]() 离子键、(非极性)共价键
离子键、(非极性)共价键
(5)NH4NO3 NH![]() +OH-
+OH-![]() NH3↑+H2O
NH3↑+H2O
(6)4Na2SO3===Na2S+3Na2SO4
【解析】A元素的原子核内只有1个质子,故A为H;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3,则B为N;C元素原子的最外层电子数比次外层多4,故C为O;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C,故D为Na;C、E同主族,且E为短周期元素,故E为S。(3)元素S、O、Na形成的简单离子的半径大小关系为S2->O2->Na+。(4)O、Na可形成化合物Na2O2,过氧化钠是由钠离子与过氧根离子通过离子键结合而成的离子化合物,电子式为Na+[![]()
![]() ]2-Na+,所含化学键为离子键和非极性共价键。(5)由H、N、O三种元素形成的离子化合物为硝酸铵,其化学式为NH4NO3;铵根离子与氢氧根离子在加热条件下反应生成氨气和水,离子方程式为NH
]2-Na+,所含化学键为离子键和非极性共价键。(5)由H、N、O三种元素形成的离子化合物为硝酸铵,其化学式为NH4NO3;铵根离子与氢氧根离子在加热条件下反应生成氨气和水,离子方程式为NH![]() +OH-
+OH-![]() NH3↑+H2O。
NH3↑+H2O。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】(1)碳酸:H2CO3,Ki1=4.3×10-7,Ki2=5.6×10-11;草酸:H2C2O4,Ki1=5.9×10-2,Ki2=6.4×10-5
0.1 mol/L Na2CO3 溶液的 pH________0.1 mol/L Na2C2O4 溶液的pH。(选填“大于”“小于”或“等于”)
等浓度草酸溶液和碳酸溶液中,氢离子浓度较大的是___________。
(2)人体血液中的碳酸和碳酸氢盐存在平衡:H++ HCO3-![]() H2CO3,当有少量酸性或碱性物质进入血液中时,血液的 pH 变化不大,用平衡移动原理解释上述现象_________________________。
H2CO3,当有少量酸性或碱性物质进入血液中时,血液的 pH 变化不大,用平衡移动原理解释上述现象_________________________。
(3)请写出Na2CO3溶液中的微粒之间的关系式:
电荷守恒______________________,
质子守恒_______________________。
(4)已知 Ag2 CrO4、AgCl 的 Ksp 分别为 2.0×10-12和 2.0×10-10。在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中的Cl-,利用Ag+与 CrO42-生成砖红色沉淀,指示到达滴定终点。当溶液中 Cl-恰好完全沉淀(浓度等于1.0×10-5 mol·L-1)时,溶液中 c(Ag+)为____________mol·L-1,此时溶液中 c(CrO42-)等于__________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种元素,它们的原子序数依次增大,但均小于18,A和B在同一周期,A的电子式为![]() ,B原子L层的电子总数是K层的3倍;0.1 mol C单质能从酸中置换出2.24 L氢气(标准状况),同时它的电子层结构变成与氖原子的电子层结构相同;D离子的半径比C离子的小,D离子与B离子的电子层结构相同。
,B原子L层的电子总数是K层的3倍;0.1 mol C单质能从酸中置换出2.24 L氢气(标准状况),同时它的电子层结构变成与氖原子的电子层结构相同;D离子的半径比C离子的小,D离子与B离子的电子层结构相同。
(1)写出A、B、C、D元素的名称:A________,B________,C________,D________。
(2)D元素在周期表中属第________周期第________族。
(3)用电子式表示A的气态氢化物的形成过程:_____________________。
(4)A和B的单质充分反应生成化合物的结构式是____________________。
(5)B与C形成的化合物是离子化合物还是共价化合物?如何证明?___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1mol碳完全燃烧后可放出393.5KJ的热量,下列热化学方程式正确的是
A.C(s)+O2(g)=CO2(g);△H=+393.5kJ/mol
B.C(s)+![]() O2(g)=CO(g);△H=-393.5kJ/mol
O2(g)=CO(g);△H=-393.5kJ/mol
C.C+O2=CO2;△H=-393.5kJ/mol
D.C(s)+O2(g)=CO2(g);△H=-393.5kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】抗酸药有效成分有:碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝、氢氧化镁等,请写出胃酸与氢氧化铝反应的化学方程式____________________________________________;再写出碳酸氢钠与胃酸反应的离子方程式_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)同温同压下,已知O2的密度为ρg/L,则CO2的密度为__________。
(2)现有下列三种气体:①32 g CH4;②约含有6.02×1023个HC1分子的氯化氢气体;③标准状况下33.6 LO2。请按物理量由小到大的顺序排列:
a.质量________(填序号,下同);
b.分子数目________
c.相同状况下气体的体积________
查看答案和解析>>
科目:高中化学 来源: 题型:
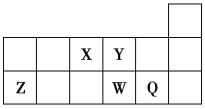
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是( )
A.离子半径的大小顺序:r(W2-)>r(Q-)>r(Y2-)>r(Z3+)
B.最高价氧化物对应水化物的酸性:W比Q的强
C.元素X的氢化物与Q的氢化物化合的产物中既含共价键又含离子键
D.X、Z、W、Q四种元素的最高价氧化物对应的水化物均能与强碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用2H++ CO32-= H2O + CO2↑表示的是
A. CH3COOH和Na2CO3的反应 B. H2SO4和碳酸氢钠的反应
C. K2CO3和NaHSO4反应 D. 碳酸钙和稀盐酸的反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com