
”¾ĢāÄæ”æÓŠ¼×”¢ŅŅĮ½Ī»Ķ¬Ń§¾łĻėĄūÓĆŌµē³Ų·“Ó¦¼ģ²ā½šŹōµÄ»ī¶ÆŠŌĖ³Šņ£¬Į½ČĖ¾łÓĆĆ¾Ę¬ŗĶĀĮʬ×÷µē¼«£¬µ«¼×Ķ¬Ń§½«µē¼«·ÅČė6 mol”¤L£1µÄH2SO4ČÜŅŗÖŠ£¬ŅŅĶ¬Ń§½«µē¼«·ÅČė6 mol”¤L£1µÄNaOHČÜŅŗÖŠ£¬ČēĶ¼ĖłŹ¾”£
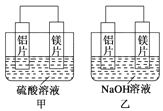
£Ø1£©Š“³ö¼×ÖŠÕż¼«µÄµē¼«·“Ó¦Ź½___________________”£
£Ø2£©ŅŅÖŠ×Ü·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ________________________”£
£Ø3£©Čē¹ū¼×ÓėŅŅĶ¬Ń§¾łČĻĪŖ”°¹¹³ÉŌµē³ŲµÄµē¼«²ÄĮĻČē¹ū¶¼ŹĒ½šŹō£¬Ōņ¹¹³Éøŗ¼«²ÄĮĻµÄ½šŹōÓ¦±Č¹¹³ÉÕż¼«²ÄĮĻµÄ½šŹō»īĘĆ”±£¬Ōņ¼×»įÅŠ¶Ļ³ö »ī¶ÆŠŌøüĒ棬¶ųŅŅ»įÅŠ¶Ļ³ö_____________»ī¶ÆŠŌøüĒ攣(ĢīŠ“ŌŖĖŲ·ūŗÅ)
£Ø4£©ÓÉ“ĖŹµŃéµĆ³öµÄĻĀĮŠ½įĀŪÖŠ£¬ÕżČ·µÄÓŠ______________”£
A£®ĄūÓĆŌµē³Ų·“ӦŊ¶Ļ½šŹō»ī¶ÆŠŌĖ³ŠņŹ±Ó¦×¢ŅāŃ”ŌńŗĻŹŹµÄ½éÖŹ
B£®Ć¾µÄ½šŹōŠŌ²»Ņ»¶Ø±ČĀĮµÄ½šŹōŠŌĒæ
C£®øĆŹµŃéĖµĆ÷½šŹō»ī¶ÆŠŌĖ³Šņ±ķŅŃ¹żŹ±£¬Ć»ÓŠŹµÓĆ¼ŪÖµĮĖ
D£®øĆŹµŃéĖµĆ÷»Æѧъ¾æ¶ŌĻóø“ŌÓ”¢·“Ó¦ŹÜĢõ¼žÓ°Ļģ½Ļ“ó£¬Ó¦¾ßĢåĪŹĢā¾ßĢå·ÖĪö
”¾“š°ø”æ£Ø1£©2H£«£«2e£==H2”ü£Ø2£©2Al£«2OH££«2H2O==2AlO2-£«3H2”ü
£Ø3£©Mg Al£Ø4£©AD
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ£Ø1£©¼×ÖŠĆ¾Ņ׏§µē×Ó×÷øŗ¼«”¢Al×÷Õż¼«£¬øŗ¼«ÉĻĆ¾·¢ÉśŃõ»Æ·“Ó¦”¢Õż¼«ÉĻĒāĄė×Ó·¢Éś»¹Ō·“Ó¦£¬Õż¼«·“Ó¦ĪŖ2H++2e-=H2”ü£¬øŗ¼«·“Ó¦ĪŖMg-2e-=Mg2+£»
£Ø2£©ŅŅ³ŲÖŠĀĮŅ׏§µē×Ó×÷øŗ¼«”¢Ć¾×÷Õż¼«£¬øŗ¼«ÉĻĀĮŹ§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬µē³Ų×Ü·“Ó¦ĪŖ£ŗ2Al£«2OH££«2H2O==2AlO2-£«3H2”ü£»
£Ø3£©¼×ÖŠĆ¾×÷øŗ¼«”¢ŅŅÖŠĀĮ×÷øŗ¼«£¬øł¾Ż×÷øŗ¼«µÄ½šŹō»īĘĆŠŌĒæÅŠ¶Ļ£¬¼×ÖŠĆ¾»ī¶ÆŠŌĒ攢ŅŅÖŠĀĮ»ī¶ÆŠŌĒ棻
£Ø4£©A”¢øł¾Ż¼×”¢ŅŅÖŠµē¼«·“Ó¦Ź½ÖŖ£¬Ōµē³ŲÕżøŗ¼«Óėµē½āÖŹČÜŅŗÓŠ¹Ų£¬¹ŹÕżČ·£»B”¢Ć¾µÄ½šŹōŠŌ“óÓŚĀĮ£¬µ«Ź§µē×ÓÄŃŅ׳Ģ¶ČÓėµē½āÖŹČÜŅŗÓŠ¹Ų£¬¹Ź“ķĪó£»C”¢øĆŹµŃé¶ŌŃŠ¾æĪļÖŹµÄŠŌÖŹÓŠŹµÓĆ¼ŪÖµ£¬¹Ź“ķĪó£»D”¢øĆŹµŃéĖµĆ÷»Æѧъ¾æ¶ŌĻóø“ŌÓ£¬·“Ó¦ÓėĢõ¼žÓŠ¹Ų£¬µē¼«²ÄĮĻĻąĶ¬Ęä·“Ó¦Ģõ¼ž²»Ķ¬µ¼ÖĀĘä²śĪļ²»Ķ¬£¬ĖłŅŌÓ¦¾ßĢåĪŹĢā¾ßĢå·ÖĪö£¬¹ŹÕżČ·£»¹ŹŃ”AD”£


 Ņ»ĻßĆūŹ¦ĢįÓÅŹŌ¾ķĻµĮŠ“š°ø
Ņ»ĻßĆūŹ¦ĢįÓÅŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢ¼ĖįÄĘŹĒŌģÖ½”¢²£Į§”¢·ÄÖÆ”¢ÖĘøļµČŠŠŅµµÄÖŲŅŖŌĮĻ”£¹¤ŅµĢ¼ĖįÄĘ(“æ¶ČŌ¼98%)ÖŠŗ¬ÓŠCa2£«”¢Mg2£«”¢Fe3£«”¢Cl£ŗĶSO42£µČŌÓÖŹ£¬Ģį“湤ŅÕĮ÷³ĢČēĻĀ£ŗ
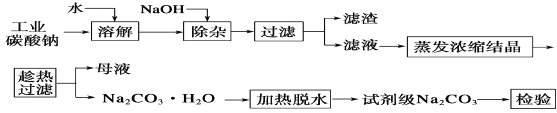
ŅŃÖŖĢ¼ĖįÄʵÄČܽā¶Č(S)ĖęĪĀ¶Č±ä»ÆµÄĒśĻßČēĻĀĶ¼ĖłŹ¾£ŗ
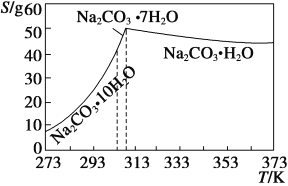
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ĀĖŌüµÄÖ÷ŅŖ³É·ÖĪŖ_______________________________”£
£Ø2£©”°³ĆČČ¹żĀĖ”±µÄŌŅņŹĒ___________________________”£
£Ø3£©ČōŌŚŹµŃéŹŅ½ųŠŠ”°³ĆČČ¹żĀĖ”±£¬æɲÉČ”µÄ“ėŹ©ŹĒ_____(Š“³öŅ»ÖÖ)”£
£Ø4£©ŅŃÖŖ£ŗNa2CO3”¤10H2O (s)===Na2CO3(s)£«10H2O(g) ¦¤H1£½ +532.36 kJ”¤mol£1
Na2CO3”¤10H2O(s)===Na2CO3”¤H2O(s)£«9H2O(g) ¦¤H2£½ +473.63 kJ”¤mol£1
Š“³öNa2CO3”¤H2OĶŃĖ®·“Ó¦µÄČČ»Æѧ·½³ĢŹ½____________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¶Ō×é³ÉÉśĪļĢåµÄ»ÆѧŌŖĖŲŗĶ»ÆŗĻĪļµÄŠšŹö£¬ÕżČ·µÄŹĒ
A. ¼”ČāĻø°ūÖŠŗ¬Įæ×ī¶ąµÄ»ÆŗĻĪļŹĒµ°°×ÖŹ
B. ×é³ÉŗĖĢĒŗĶŗĖĖįµÄ»ÆѧŌŖĖŲĶźČ«ĻąĶ¬
C. ĆøŗĶŗĖĖį¶¼ŹĒŗ¬ÓŠNŌŖĖŲµÄÉśĪļ“ó·Ö×Ó
D. ČĖ”¢¶ÆĪļÓėÖ²ĪļĖłŗ¬µÄ»ÆѧŌŖĖŲµÄÖÖĄą²īŅģŗÜ“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµŃéŠčŅŖ0£®80 mol”¤L-1NaOHČÜŅŗ475 mLŗĶ0£®40 mol”¤L-1ĮņĖįČÜŅŗ500 mL”£øł¾ŻÕāĮ½ÖÖČÜŅŗµÄÅäÖĘĒéæö»Ų“šĻĀĮŠĪŹĢā£ŗ
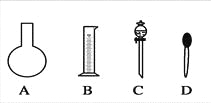
£Ø1£©ČēĶ¼ĖłŹ¾µÄŅĒĘ÷ÖŠÅäÖĘČÜŅŗæĻ¶Ø²»ŠčŅŖµÄŹĒ________£ØĢīŠņŗÅ£©£¬ÅäÖĘÉĻŹöČÜŅŗ»¹ŠčÓƵ½µÄ²£Į§ŅĒĘ÷ŹĒ________£ØĢīŅĒĘ÷Ćū³Ę£©”£
£Ø2£©ĻĀĮŠ²Ł×÷ÖŠ£¬²»ÄÜÓĆČŻĮæĘæŹµĻÖµÄÓŠ______________£ØĢīŠņŗÅ£©”£
A£®ÅäÖĘŅ»¶ØĢå»ż×¼Č·ÅØ¶ČµÄ±ź×¼ČÜŅŗ |
B£®ĮæČ”Ņ»¶ØĢå»żµÄŅŗĢå |
C£®²āĮæČŻĮæĘæ¹ęøńŅŌĻĀµÄČĪŅāĢå»żµÄŅŗĢå |
D£®×¼Č·Ļ”ŹĶijŅ»ÅØ¶ČµÄČÜŅŗ |
E£®Öü“ęČÜŅŗ
F£®ÓĆĄ“¼ÓČČČܽā¹ĢĢåČÜÖŹ
£Ø3£©øł¾Ż¼ĘĖćÓĆĶŠÅĢĢģĘ½³ĘČ”NaOHµÄÖŹĮæĪŖ___________g”£ŌŚŹµŃéÖŠĘäĖū²Ł×÷¾łÕżČ·£¬Čō¶ØČŻŹ±ø©ŹÓæĢ¶ČĻߣ¬ŌņĖłµĆČÜŅŗÅضČ_________£ØĢī”±“óÓŚ”±”¢”°µČÓŚ”±»ņ”°Š”ÓŚ”±£¬ĻĀĶ¬£©0£®8 mol”¤L-1”£Čō¶ØČŻŹ±£¬ÓŠÉŁŠķÕōĮóĖ®Č÷ĀäŌŚČŻĮæĘæĶā£¬ŌņĖłµĆČÜŅŗÅضČ__________0.8 mol”¤L-1”£
£Ø4£©øł¾Ż¼ĘĖćµĆÖŖ£¬ĖłŠčÖŹĮæ·ÖŹżĪŖ98 %”¢ĆܶČĪŖ1£®84 mol”¤L-1µÄÅØĮņĖįµÄĢå»żĪŖ__________mL£Ø¼ĘĖć½į¹ū±£ĮōŅ»Ī»Š”Źż£©”£Čē¹ūŹµŃéŹŅÓŠ10 mL”¢15 mL”¢20 mL”¢50 mLĮæĶ²£¬Ń”ÓĆ___________mLĮæĶ²×īŗĆ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŖĮĖ½«»ģÓŠK2SO4”¢MgSO4µÄKNO3¹ĢĢåĢį“棬²¢ÖĘµĆ“æ¾»µÄKNO3ČÜŅŗ£¬Ä³Ķ¬Ń§Éč¼ĘČēĻĀŹµŃé·½°ø£ŗ

£Ø1£©²Ł×÷¢ŁĪŖ____________£»
£Ø2£©²Ł×÷¢Ś”«¢Ü¼ÓČėµÄŹŌ¼ĮæÉŅŌĪŖ ”£
£Ø3£©ČēŗĪÅŠ¶ĻSO![]() ŅŃ³ż¾”£¬¼ņŹöŹµŃé²Ł×÷ £»
ŅŃ³ż¾”£¬¼ņŹöŹµŃé²Ł×÷ £»
£Ø4£©ŹµŃé¹ż³ĢÖŠ²śÉśµÄ¶ą“Ī³Įµķ_________(Ģī”°ŠčŅŖ”±»ņ”°²»ŠčŅŖ”±)¶ą“Ī¹żĀĖ£¬ĄķÓÉ ”£
(5)øĆĶ¬Ń§Éč¼ĘµÄŹµŃé·½°ø____________(Ģī”°ŗĻĄķ”±»ņ”°²»ŗĻĄķ”±)£¬ĄķÓÉŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
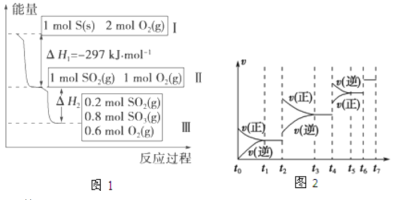
”¾ĢāÄæ”æŌŚŅ»øöĪĀ¶ČŗĶĢå»ż²»±äµÄČŻĘ÷ÖŠ£¬ĮņæÉŅŌ·¢ÉśČēĻĀ±ä»Æ£¬Ęä·“Ó¦¹ż³ĢŗĶÄÜĮæ¹ŲĻµČēĶ¼1ĖłŹ¾”££ØSO2(g)+1/2O2(g)![]() SO3(g) ”÷H=£98.45kJ”¤mol£1£©
SO3(g) ”÷H=£98.45kJ”¤mol£1£©
£Ø1£©ĮņČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø2£©ŗćČŻĢõ¼žĻĀ£¬ĻĀĮŠ“ėŹ©ÖŠÄÜŹ¹n(SO3)/n(SO2)±ČĶ¼1ĖłŹ¾ĒéæöŌö“óµÄÓŠ ”£
A£®½µµĶĪĀ¶Č B£®³äČėHe C£®ŌŁ³äČė1mol SO2(g)ŗĶ1mol O2(g) D£®Ź¹ÓĆ“ß»Æ¼Į
£Ø3£©ŗćĪĀŗćČŻŹ±£¬Ķ¼1ÖŠIIµ½III·“Ó¦·Å³öµÄČČĮæ±Č1mol SO2ŗĶ2mol O2³ä·Ö·“Ó¦·Å³öµÄČČĮæ £ØĢī
”°“ó”±”¢”°Š””±»ņ”°ĻąµČ”±£©”£
£Ø4£©Ä³SO2(g)ŗĶO2(g)ĢåĻµ£¬Ź±¼ät1“ļµ½Ę½ŗāŗó£¬øıäijŅ»Ķā½ēĢõ¼ž£¬·“Ó¦ĖŁĀŹvÓėŹ±¼ätµÄ¹ŲĻµČēĶ¼2ĖłŹ¾£¬Čō²»øıäSO2(g)ŗĶO2(g)µÄĮ棬ŌņĶ¼ÖŠt2Ź±ŅżĘšĘ½ŗāŅĘ¶ÆµÄĢõ¼žæÉÄÜŹĒ £»Ķ¼ÖŠ±ķŹ¾Ę½ŗā»ģŗĻĪļÖŠSO3µÄŗ¬Įæ×īøßµÄŅ»¶ĪŹ±¼äŹĒ ”££ØČēt1”«t2”¢t3”«t4”¢t5”«t6”¢t6”«t7µČ£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆH2æɽ«¹¤Ņµ·ĻĘųÖŠµÄNO“߻ƻ¹Ō³ÉN2£¬ĘäĖūĮæ×Ŗ»Æ¹ŲĻµČēĶ¼(Ķ¼ÖŠ¼ĘĮ浄Ī»ĪŖmol), Ōņ£ŗNO(g)+H2(g)=![]() N2(g)+H2O(g)µÄ”÷HĪŖ£Ø £©
N2(g)+H2O(g)µÄ”÷HĪŖ£Ø £©

A£®0.5(a+b-c-d)kJ/mol B£®0.5(c+a-d-b)kJ/mol
C£®0.5(c+d-a-b)kJ/mol D. 0.5(c+d-a-b)kJ/mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĄė×Ó·½³ĢŹ½ÖŠÕżČ·µÄŹĒ ( )
A£®¹¤ŅµÉĻ“Ö¹čµÄÖʱø£ŗSiO2£«C![]() Si+CO2”ü
Si+CO2ӟ
B£®Cu2OÓėĻ”H2SO4·“Ó¦£ŗCu2O£«2H+=2Cu+£«H2O
C£®ÓĆĻ”ĻõĖįĻ“µÓŹŌ¹ÜÄŚ±ŚµÄŅų¾µ£ŗ3Ag+4H++NO3£=3Ag++NO”ü+2H2O
D.ĻņMg(HCO3)2ČÜŅŗÖŠ¼Ó×ćĮæÉÕ¼īČÜŅŗ:Mg2£«+2HCO3£+2OH£=MgCO3”ż+2H2O+CO32£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĘųĢ¬Ēā»ÆĪļÖŠ£¬×ī²»ĪČ¶ØµÄŹĒ£Ø £©
A. HI B. HBr C. HCl D. HF
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com