
| A. | 12.0% | B. | 14.3% | C. | 19.0% | D. | 66.7% |
分析 容积可变的密闭容器中,发生N2+3H2$\stackrel{一定条件}{→}$2NH3,
开始 (mol) 2 8 0
转化(mol) 0.8 2.4 1.6
平衡(mol) 1.2 5.6 1.6
根据物质的量之比等于体积之比来计算平衡时的氮气的体积分数.
解答 解:容积可变的密闭容器中,发生N2+3H2$\stackrel{一定条件}{→}$2NH3,
开始 (mol) 2 8 0
转化(mol) 0.8 2.4 1.6
平衡(mol) 1.2 5.6 1.6
则平衡时氮气的体积分数为$\frac{1.2}{1.2+5.6+1.6}×100%$=14.3%,
故选B.
点评 本题考查化学平衡的计算,为高频考点,侧重于学生的分析、计算能力的考查,明确三段法计算及物质的量之比等于体积之比的关系即可解答,题目难度不大.


科目:高中化学 来源: 题型:实验题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡后CO的体积分数为40% | |
| B. | 平衡后CO的转化率为25% | |
| C. | 平衡后水的转化率为50% | |
| D. | 平衡后混合气体的平均相对分子质量为24 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ①④⑤ | C. | ②③④ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 它的一氯代物只有一种同分异构体 | |
| B. | 它的二氯代物有两种同分异构体 | |
| C. | 它的分子式为C8H8 | |
| D. | 它与苯乙烯(C6H5-CH=CH2)互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
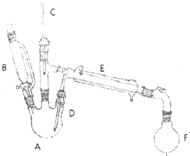 溴乙烷是有机合成的重要原料,实验室合成溴乙烷的装置示意图、相关原理和数据如下:
溴乙烷是有机合成的重要原料,实验室合成溴乙烷的装置示意图、相关原理和数据如下:| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解度 | |
| 乙醇 | 46 | 0.789 | 78.3 | 易溶 |
| 溴乙烷 | 109 | 1.46 | 38.2 | 难溶 |
| 浓硫酸(H2SO4) | 98 | 1.84 | 338.0 | 易溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com