
| A�������Թ���Һ����ɫ�������Թ���Һһ����Ѫ��ɫ |
| B�������Թ���Һ����ɫ�������Թ���Һ�������������� |
| C�����Թ���Һ��Ѫ��ɫ������Թ���Һ�����ܳ���ɫ |
| D�����Թ���Һ����ɫ�����Թ����Ϻ�ɫ��ȥ��˵���μ���ˮ�����Һ��һ������Fe3+��Fe2+ |


 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д� �����ܿ����ϵ�д�
�����ܿ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��HCO3-��ˮ�ⷽ��ʽ�ɱ�ʾΪ��HCO3-+H2O?H3O++CO32- |
| B����NaHCO3��Һ�м�������ij���ʯ��ˮ�����ְ�ɫ������2HCO3-+Ca2++2OH-�TCaCO3��+CO32-+2H2O |
| C����NaAlO2��Һ��ͨ�����CO2��Al��OH��3��2AlO2-+CO2+3H2O=2Al��OH��3��+CO32- |
| D����16.8g ����Ͷ��100mL 4.0mol/L��HNO3��Һ�У���ԭ����ֻ��NO��3Fe+8 H++2NO3-=3Fe2++2NO��+4H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 3 |
| 2 |
| 3 |
| �¶�/�� | 1000 | 1150 | 1300 |
| ƽ�ⳣ�� | 4.0 | 3.7 | 3.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
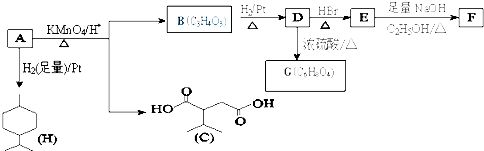
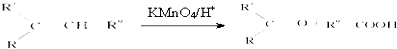
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| c(H+) |
| c(OH-) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com